Forschung
Neuer Ansatz für die Therapie bei Diabetes?
Forschern ist es gelungen, Immunreaktionen im Frühstadium des Typ-1-Diabetes einzufangen.
Veröffentlicht: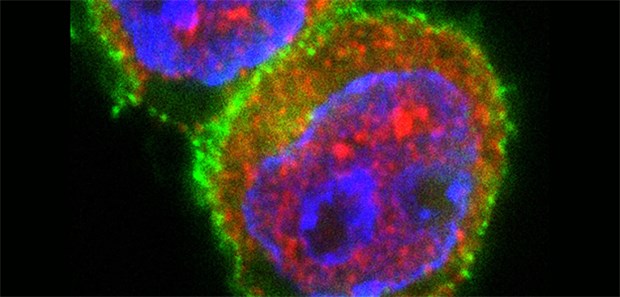
T-Zellen nach Stimulation in Gegenwart von miRNA181a. Immunfluoreszenzfärbung von T-Zellen (grün: T-Zellmarker CD4, rot: Transkriptionsfaktor NFAT5, blau: Zellkern). Die Stimulation der T-Zellen in Gegenwart eines miRNA181a mimics resultiert in einer deutlich erhöhten NFAT5-Expression in den T-Zellen.
© Helmholtz Zentrum München
MÜNCHEN. Forscher am Helmholtz Zentrum München haben einen Mechanismus entdeckt, der die Autoimmunreaktion in einem Frühstadium des Typ-1-Diabetes verstärkt. Blockierten sie die zugehörigen Moleküle, war das Immunsystem deutlich weniger aktiv (Science Translational Medicine 2018; online 3. Januar).
Bei den zu Typ-1-Diabetes führenden Prozessen sind regulatorische T-Zellen (Tregs) von besonderer Bedeutung, erinnert das Forschungszentrum in einer Mitteilung zur Studie: Sie unterdrücken bei Gesunden überschießende Immunreaktionen und verhindern so Autoimmunerkrankungen.
"In der Arbeit konnten wir einen Mechanismus aufklären, der dazu führt, dass in einem Frühstadium des Typ-1-Diabetes weniger Tregs produziert werden und das Immunsystem deshalb unkontrollierter um sich greifen kann", wird Dr. Carolin Daniel zitiert, Gruppenleiterin am Institut für Diabetesforschung (IDF) des Helmholtz Zentrums München und Forscherin im DZD. Maßgeblich daran beteiligt seien die Moleküle miRNA181a und NFAT5: Im frühen Stadium des Typ-1-Diabetes führt miRNA181a zur Aktivierung des Transkriptionsfaktors NFAT5. Die Folge ist eine Hemmung der Tregs und dadurch eine verstärkte Immunaktivierung.
Um zu prüfen, inwiefern sich die neue Erkenntnis für mögliche Therapieansätze eignet, arbeiteten die Forscher um Erstautorin Isabelle Serr an einem präklinischen Modell mit bestehender Inselautoimmunität. Unterbrachen sie die miRNA181a/NFAT5-Achse, kam es zu signifikant geringerer Aktivierung des Immunsystems und vermehrter Bildung von Tregs, berichtet das Helmholtz Zentrum. Das sei sowohl durch die pharmakologische Hemmung von miRNA181a als auch von NFAT5 gelungen. "Die gezielte Inhibierung von miRNA181a oder NFAT5 könnte neue Wege eröffnen, die Aktivität des Immunsystems gegen die eigenen Inselzellen zu verringern", kommentiert Professor Anette-Gabriele Ziegler, Direktorin des IDF. "Auch die Kombination mit anderen immunmodulierenden Ansätzen wäre, perspektivisch gesehen, ein denkbarer Interventionsversuch."
Künftig wollen die Wissenschaftler die vorliegenden Befunde in präklinischen Tests untersuchen. Hierzu soll in humanisierten Modellen geprüft werden, ob die Kombination aus Insulinimpfung und Hemmung der miRNA181a/NFAT5-Achse dazu führt, dass das Immunsystem gegenüber den Insulin-produzierenden Zellen toleranter wird.(eb)




