Gliome
Der Tumorgrad bestimmt die Therapie
Gliom-Therapie so oder so: Schon bei Grad-III-Tumoren ist jetzt eine Radiochemotherapie angebracht. Bei niedrigmalignen Gliomen bleibt dagegen kontrolliertes Abwarten eine Option.
Veröffentlicht: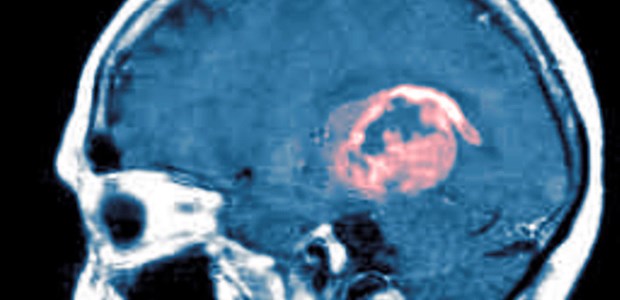
Beim Gliom erfordern Langzeitdaten großer Studien nun neue Therapiestrategien.
© Dr. Matthias Eberhardt/Arteria Photography
MAINZ. Wann sollten Ärzte bei Gliomen zum Messer greifen, wann die Röntgenkanonen anschalten und wann einen Cocktail von Zytostatika verabreichen? Langzeitdaten großer Studien erfordern nun neue Therapiestrategien.
Welche Verfahren demnach am meisten versprechen, hat Professor Uwe Schlegel von der Neurologischen Klinik der Universität Bochum auf der Ärztefortbildung "Neuro Update" erläutert.
Schneiden oder unter strenger Kontrolle abwarten, ob es zur Progression kommt - das ist die Frage bei niedrigmalignen Gliomen (WHO-Grad II). Solche Grad-II-Gliome verursachen oft nur epileptische Anfälle, die sich gut kontrollieren lassen.
Daher muss sorgfältig abgewogen werden, ob die Therapie dem Patienten mehr schadet als nützt. Bislang gibt es aber keine prospektiv randomisierten Studien zum Nutzen der Resektion.
Untersuchungen deuten aber auf einen Vorteil bei der Lebenszeit, wenn sich mindestens 90 Prozent der Tumormasse gefahrlos entfernen lassen.
Mehr Überlebenszeit bei Resektion
Ein norwegischer Vergleich zwischen zwei Zentren, in denen eines die Resektion und das andere kontrolliertes Abwarten favorisierte, ergab mit 5,9 versus 7 Jahren zudem einen Vorteil für die Resektion bei der medianen Überlebenszeit.
Schlegels Fazit: Wie bisher nur dann operieren, wenn sich das Tumorgewebe in der Bildgebung klar abgrenzen lässt und ohne die Gefahr neurologischer Defizite zu mindestens 90 Prozent entfernt werden kann. Von Teilresektionen rät er ab.
Bei anaplastischen Gliomen (Grad III) gibt es die gravierendsten Änderungen. Biopsie und Resektion sind Konsens, doch was dann? Erst Radiatio, dann beim unvermeidlichen Rezidiv die Chemotherapie, genau umgekehrt oder von Anfang an gleich beides?
Fünfjahresdaten der Studien EORTC 26951 und RTOG 94-02 hatten zunächst keinen Vorteil bei der Überlebenszeit für eine kombinierte Radiochemotherapie im Vergleich zu einer alleinigen Radiatio nach der Resektion ergeben. Bei der Chemotherapie wurde hier ein Cocktail aus Procarbazin, CCNU und Vincristin (PCV) verwendet.
Schließlich ergab die Studie NOA-04, dass es auch egal ist, ob man mit einer Radiatio beginnt und dann beim Rezidiv zur Chemotherapie greift oder umgekehrt. Ebenso war es für die Überlebenszeit ohne Bedeutung, ob man für die Chemotherapie PCV oder Temozolomid nahm.
Als Konsequenz setzte sich nach 2009 in Deutschland die alleinige initiale Chemotherapie mit dem besser verträglichen Temozolomid nach der Resektion durch, so Schlegel.
Radiochemotherapie hat Vorteile
Von diesem Vorgehen muss man sich nun verabschieden, so der Neuroonkologe, denn jetzt sind Zwölfjahresdaten der EORTC- und RTOG-Studien bekannt geworden, und die zeigen ganz klar: Nach fünf bis sechs Jahren gehen die Kurven für die Überlebensraten auseinander - die kombinierte Radiochemotherapie hat deutliche Vorteile.
Besonders drastisch zu erkennen ist dies bei Patienten mit einer Kodeletion der Chromosomenabschnitte 1p / 19q in den Tumorzellen. Diese haben generell eine bessere Prognose.
In der RTOG-Studie mit einer Beobachtungszeit von bis zu 18 Jahren betrug die mediane Überlebenszeit solcher Patienten mit initialer Radiochemotherapie 14,7 Jahre, mit initialer Radiatio nur 7,3 Jahre.
Doch auch ohne die Kodeletion zeigten sich Vorteile: Nach zehn Jahren lebten mit der Radiochemotherapie noch 25 Prozent der Patienten, mit initialer Radiatio nur etwa 10 Prozent (J Clin Oncol 30, 2012, suppl; abstr 2008b und J Clin Oncol 30, 2012, suppl; abstr 2).
Nach diesen Daten wäre die beste evidenzbasierte Behandlung bei Grad-III-Gliomen eine konkomitante Radiochemotherapie mit zweimal 30 Gy sowie vier bis sechs Zyklen PCV, so Schlegel.
Ob sich PCV durch Temozolomid ersetzen lässt, könne derzeit nicht gesagt werden. Schlegel rät, auf das recht toxische Vincristin zu verzichten, da es Hinweise gebe, dass eine PC-Therapie ähnlich effektiv sei.
Alte Menschen - schlechte Prognose
Standard beim Glioblastom (Grad IV) sind Biopsie und Resektion gefolgt von einer konkomitanten Radiochemotherapie mit Temozolomid plus sechs Zyklen einer adjuvanten Temozolomid-Therapie. Dies gilt bis zum 65. Lebensjahr, bei gutem klinischem Zustand bis zum 70. Jahr.
Da mit dem Alter die Prognose schlechter wird und häufiger schwere Nebenwirkungen bei einer Chemotherapie zu befürchten sind, wird bei alten Menschen nach der Op oft nur noch bestrahlt.
Diese Prozedur dauert aber fast zwei Monate und kostet daher viel der noch verbliebenen Lebenszeit. Daher überlegt man sich, ob die Radiotherapie durch Temozolomid ersetzt werden kann.
In der deutschen NOA-08-Studie war Temozolomid der Radiotherapie nicht unterlegen. Bei MGMT-Methylierern konnte die Überlebenszeit mit Temozolomid sogar fast verdoppelt werden (8,3 vs. 4,6 Monate), hingegen war sie ohne MGMT-Methylierung etwas schlechter als die Radiatio (3,3 vs. 4,6 Monate).
Für Schlegel ergibt sich die Konsequenz, dass der MGMT-Status bestimmt werden muss und bei Methylierern eine Chemotherapie erfolgt.




