Weltkrebstag
Aufbruchstimmung in der Krebsmedizin
Die personalisierte Krebsmedizin erlebt derzeit eine Goldgräberstimmung. Angetrieben wird sie vor allem durch die rasante Entwicklung bei der Genom-Entschlüsselung. Wir ziehen zum Weltkrebstag Bilanz.
Veröffentlicht:
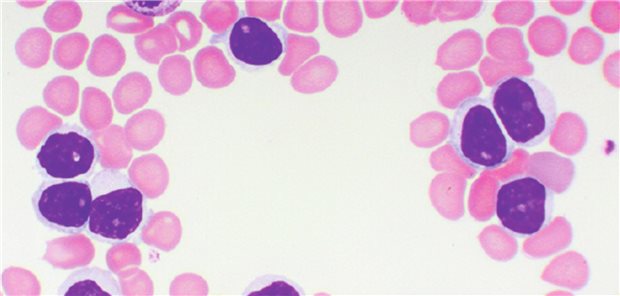
Auffälliges Gewebe: Wird die Personalisierung die Onkologie beflügeln?
© Friso Gentsch / dpa
HEIDELBERG. Die personalisierte Medizin ist in der Krebsmedizin bisher am weitesten fortgeschritten. Das führt ein Blick auf die aktuelle vfa-Liste der derzeit für diese gezielte Behandlung zugelassenen Medikamente klar vor Augen.
Inzwischen sind es insgesamt 29 Medikamente, die in Deutschland auf dem Markt sind, bei denen vor der Anwendung geprüft werden muss oder bei denen der Test empfohlen wird, ob die genetische Konstellation für einen optimalen Therapieerfolg mit minimalen Nebenwirkungen stimmt.
Allein 19 davon sind Krebsmedikamente. Den Reigen dieser modernen Therapeutika eröffnet haben der Antikörper Trastuzumab (mit Pflichttest auf HER2/neu) gegen Brustkrebs und der Tyrosinkinasehemmer Imatinib (Pflichttest auf das Philadelphia-Chromosom) gegen chronische myeloische Leukämie.
Die moderne molekulargenetische Diagnostik ist somit ein Grundpfeiler der personalisierten - oder besser stratifizierten - Krebsmedizin: die gezielte Therapie bei einer bestimmten Gruppe von Patienten, von denen man aufgrund von Tests weiß, dass die Behandlung erfolgreich sein wird.
Ganz wesentliche Erkenntnisse sind aus den genetischen Analysen von Krebszellen zu erwarten. Dabei beschränken sich die Wissenschaftler nicht mehr auf die Sequenzierung einzelner Gene, sondern es geht um die Totalsequenzierung des Krebsgenoms einzelner Patienten.
Inzwischen sind die technischen Voraussetzungen so weit fortgeschritten, dass in der Regel nach zwei Tagen die komplette Sequenz vorliegt, wie der Molekulargenetiker Professor Peter Lichter vom Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg bei einem Workshop im Zentrum berichtete. Das DKFZ verfügt über 13 solcher Sequenziermaschinen.
Seit 2010 beteiligen sich deutsche Forscher mit drei Projekten an dem ehrgeizigen internationalen Vorhaben des International Cancer Genome Consortium (ICGC) mit derzeit insgesamt 51 Forschungsprojekten. Geplant ist, im ICGC insgesamt 50.000 Krebsgenome vollständig zu sequenzieren.
In dem von Lichter koordinierten PedBrain-Projekt sollen mehr als 250 Medulloblastome und mehr als 250 niedrigmaligne, pilozytische Astrozytome bei Kindern analysiert werden. Die Hälfte sei inzwischen erreicht, so Lichter.
Neue Herausforderung: Riesige Datenmengen
Bei der Totalsequenzierung der Krebsgenome von Kindern mit Medulloblastomen entdeckten die Wissenschaftler mehr als 760 Mutationen in fast 600 Genen (Nature 2012; 488: 100-105). Dabei spürten sie auch Mutationen auf, die bisher nicht im Zusammenhang mit dem Hirntumor standen.
Um die routinemäßige Anwendung der Gesamtgenomanalyse im klinischen Alltag des Nationalen Centrums für Tumorerkrankungen (NTC) Heidelberg zu fördern, wurde die Initiative DKFZ-HIPO (Heidelberg Center for Personalized Oncology) gegründet.
Sie bündelt das Experten-Know-how im Bereich der Genomanalyse, Bioinformatik und klinische Onkologie innerhalb des DKFZ und des NCT.
Die umfangreichen Ergebnisse der Totalsequenzierung werfen aber auch die Frage auf, wann man bei der Krebsdiagnostik die Histologie verlassen und sich ganz der Molekulargenetik zuwenden kann.
Dies würde eine völlig neue Klassifikation auf der Grundlage der DNA begründen. Ob das eines Tages möglich sein wird, soll bei kindlichen Hirntumoren überprüft werden.
Die Totalsequenzierung der Krebsgenome förderte bereits einige Überraschungen zutage. So entdeckten Heidelberger Forscher am DKFZ erstmals in Medulloblastomen eine chromosomale Instabilität, die in 2 bis 3 Prozent aller Tumoren vorkommt und als Chromothripsis bezeichnet wird: Ein Chromosom wird in viele kurze Fragmente zerstückelt, die durch die Reparaturmechanismen der Zelle nicht mehr korrekt zusammengesetzt werden und zum Teil verloren gehen.
In der Folge entartet die Zelle. Mutationen im Gen p53, auch als Wächter des Genoms bekannt, prädisponieren offenbar zur Chromothripsis.
So ist es sinnvoll, bei bestimmten Medulloblastomformen gezielt nach p53-Mutationen zu fanden, um frühzeitig die Therapie danach auszurichten, weil zum Beispiel die Strahlentherapie die DNA weiter schädigen würde - ebenfalls eine Form der personalisierten Medizin.
Durch die im Zusammenhang mit den Totalsequenzierungen anfallenden Riesenmengen an Daten wird die Speicherung zur Herausforderung. Lichter: "Die Datenspeicherung habe ich unterschätzt."
Bisher wurden bereits Daten in der Größenordnung von sechs Petabyte (sechs Millionen Gigabyte) zusammengetragen. Allein das DKFZ stellt etwa 1,2 Petabyte Speicherplatz zur Verfügung.
Was tun mit den "Zufallsbefunden" der Genomanalyse?
Die Sequenzierung von Krebsgenomen löst auch Diskussionen über die ethischen und juristischen Aspekte aus.
Durch die komplette Sequenzierung von Genomen der Krebszellen erhoffen sich die Wissenschaftler, Veränderungen im Vergleich zum Genom gesunder Zellen zu entdecken, die sich für die Diagnostik und als neue Zielstrukturen für Arzneien der personalisierten Medizin nutzen lassen. Doch wirft diese Sequenzierung auch ethische und juristische Fragen auf.
Wie soll ein Forscher, der durch die Sequenzierung einen tiefen Einblick in das Genom eines Patienten erhält, mit dem Wissen umgehen? Wie soll ein Patient über mögliche Zufallsbefunde, die nicht den Tumor betreffen, aufgeklärt werden - etwa bei einer Veranlagung für Chorea Huntingtonoder Amyotrophe Lateralsklerose?
Nicht geklärt ist außerdem, welche Daten gespeichert werden sollen. Und: Wer darf überhaupt darüber entscheiden, was gespeichert wird und wie lange? Wer hat Zugang zu diesen Daten?
Die Herausforderung fängt bereits mit der Einverständniserklärung der Patienten an, wie Professor Peter Lichter, Leiter der Abteilung Molekulare Genetik am Deutschen Krebsforschungszentrum (DKFZ) bei einer Veranstaltung am Zentrum in Heidelberg sagte. Denn gegenwärtige Erklärungen schließen noch nicht ein, dass es die Möglichkeit der Reidentifizierung einer Person gibt.
Es werden deshalb neue Einverständniserklärungen nötig sein. Die Patienten müssen zudem über den Umfang der genetischen Analysen aufgeklärt werden. Die einfache Angabe, es handele sich um eine "genetische Analyse", reicht dann nicht mehr aus.
Der Wunsch der Patienten nach Information über ihr Erbgut, aber auch auf Nichtwissen muss berücksichtigt und in dem Aufnahmeformular entsprechend festgelegt werden.
Ein anderer noch nicht geklärter Aspekt: Naturwissenschaftler haben als Nichtmediziner keinen Schutz wie Experten in anderen Disziplinen: Es gibt für sie nicht wie etwa bei Juristen, Theologen und Ärzten einen Kodex, nach dem Informationen nicht weitergegeben, aber auch nicht angefordert werden dürfen, etwa von der Polizei. Ein entsprechender Kodex für Naturwissenschaftler wird derzeit erarbeitet.
Den bisher unbeantworteten Fragen wird im interdisziplinären Marsilius-Projekt "Ethische und rechtliche Aspekte der Totalsequenzierung des menschlichen Genoms" (EURAT) nachgegangen. Die Universität Heidelberg finanziert das Projekt. Beteiligt sind Juristen, Theologen, Ethiker, Informatiker und Kliniker.
Lichter: "Im Moment wird ein Zwischenabschluss vorbereitet. Es wird darin ein Heidelberger Weg beschrieben." Er könne als Vorschlag für andere Wissenschaftler dienen. Die Stellungnahme soll noch in diesem Jahr vom Marsilius-Kolleg veröffentlicht werden.
Wie wichtig solche Empfehlungen sind, belegen die Aktivitäten bei der Genomsequenzierung. So ist geplant, am Nationalen Centrum für Tumorerkrankungen (NCT) in Heidelberg bis 2015 bei jedem der dort jährlich etwa 10.000 Krebspatienten eine Totalsequenzierung des Krebsgenoms vorzunehmen.
Nach Angaben von Professor Otmar Wiestler, Vorstandsvorsitzender und Wissenschaftlicher Vorstand am DKFZ, könnten noch in diesem Jahr bis 2000 solcher Analysen möglich sein.
Das 2011 gegründete Heidelberger Zentrum für personalisierte Onkologie (HIPO) soll den Prozess der Individualisierung beschleunigen. Es ruht auf Genomik, Bioinformatik und klinischer Onkologie im NCT. 26 Projekte zu 14 Tumorentitäten wie Brustkrebs, Pankreaskarzinom, Dickdarm-, Magen- und Lungenkrebs wurden bereits begonnen.