Leitartikel zur Krebstherapie
Mammutprojekt Personalisierung
Die personalisierte Krebsmedizin verspricht eine Therapie, die sich an den molekularen Eigenheiten des Tumors ausrichtet. Das klingt nach der großen Verheißung der modernen Onkologie. Doch einfacher wird die Behandlung dadurch sicher nicht.
Veröffentlicht:
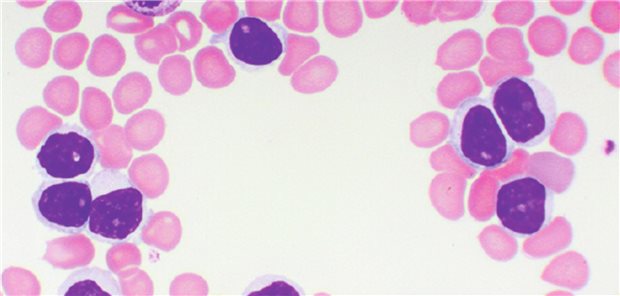
Diagnostik bringt Licht ins Genom: Welche Gene sind mit im Spiel, die die Krebstherapie beeinflussen könnten?
© Danielle Bonardelle / fotolia.com
An der Universität Heidelberg startet demnächst ein Projekt, das nicht nur deutschlandweit bisher einmalig ist. Ab 2015 soll dort bei allen Krebspatienten eine Komplettsequenzierung des Tumorgenoms erfolgen. Dabei kommen so genannte Next-Generation-Sequencing-Technologien (NGS) zum Einsatz, also Roboter, die die Genausstattung eines Tumors schnell und erstaunlich preiswert ermitteln.
Diese "Rohdaten" werden in eine Software eingespeist, die mit modernen Datenbanktechnologien arbeitet und die den Ärzten bei der Auswahl der Therapien helfen soll.
Das Konzept ist zwar nicht mehr ganz neu. Aber es bleibt faszinierend, weil es darauf angelegt ist, die klassische, strikt organbezogene Onkologie hinter sich zu lassen. Nicht umsonst ließ sich der Mäzen Dietmar Hopp davon überzeugen, eine Anschubfinanzierung von 15 Millionen Euro zur Verfügung zu stellen.
Zur Wahrheit gehört aber auch: Dieser Paradigmenwechsel ist kein Selbstläufer. Die klinische Evaluierung beispielsweise ist nicht ganz trivial: Organorientierte Standardtherapien müssten gegen einen auf molekularer Tumoranalytik basierenden Therapiealgorithmus antreten.
Nicht unmöglich, aber auch nicht einfach, schon deswegen nicht, weil "simple" Personalisierungskonzepte wie die Bestimmung von Her2-, KRAS- oder ALK-Status längst Bestandteil vieler Standardtherapien sind.
Die personalisierte Krebsmedizin hat aber nicht nur Studienprobleme, auch Erkenntnisprobleme. Da ihr Erfolg wesentlich darauf beruht, zu verhindern, dass sich resistente Tumorzellen entwickeln, die sich der therapeutischen Suppression entziehen, müssten die Resistenzmechanismen eigentlich sehr viel genauer bekannt sein, als das bisher der Fall ist.
Das Idealszenario wären biomathematische Modelle, anhand derer sich das Resistenzverhalten von Tumorzellen in Abhängigkeit von bestimmten Therapiekombinationen vorhersagen lässt. Davon ist die Krebsmedizin weit entfernt.
Studien: Personalisierung ist kompliziert
Bei einer Veranstaltung der Charité Berlin anlässlich des Kongresses der American Society of Clinical Oncology (ASCO 2014) wurde das Dilemma der Personalisierung erneut deutlich. Beispiel metastasiertes kolorektales Karzinom (mCRC): In der europäischen FIRE 3-Studie war eine Anti-EGFR-Therapie der Anti-VEGF-Therapie (in Kombination mit einer FOLFIRI-Chemotherapie*) bei Patienten mit mCRC ohne KRAS-Mutationen hinsichtlich des progressionsfreien Überlebens (PFS) um knapp vier Monate überlegen.
Wurden noch andere RAS-Mutationen berücksichtigt, stieg der Vorteil auf acht Monate. Die beim ASCO vorgestellte CRYSTAL-Studie fand bei RAS-Wildtyp-Patienten ebenfalls acht Monate Vorteil für die zusätzliche Anti-EGFR-Therapie gegenüber FOLFIRI alleine.
Dies bestätige Personalisierungskonzepte und spreche für die Ausweitung der RAS-Tests beim mCRC über KRAS hinaus, betonte der Charité-Onkologe Professor Hanno Riess. Leider gab es dann beim ASCO aber auch noch die CALGB/SWOG 80405-Studie, die das Design der FIRE 3-Studie replizierte und keinen Unterschied beim PFS fand.
Ein möglicher Grund sei, dass bei der Chemotherapie neben FOLFIRI auch FOLFOX** erlaubt war, so Riess. Das ist aber noch nicht abschließend geklärt. Niemand zweifelt an der Relevanz der RAS-Tests. Aber klar ist auch: Irgendetwas in der CALBG-Studie machte die schon als gesetzt geltenden Vorteile der RAS-Personalisierung zunichte. Nur was?
Sagen Gene wirklich die ganze Wahrheit?
Professor Ulrich Keilholz, Leiter des Comprehensive Cancer Centers der Charité, hatte noch ein Beispiel parat. Patienten mit malignem Melanom und Mutation im BRAF V600-Gen profitieren massiv von der BRAF-Hemmung mit Vemurafenib oder Dabrafenib. Es kommt aber stets zur Progredienz, weil die Melanomzellen Resistenzen entwickeln.
Vor diesem Hintergrund wird die Kombination mit MEK-Inhibitoren in Studien evaluiert. Sie greifen in denselben Signalweg wie die BRAF-Inhibitoren ein und blockieren dort einen möglichen Resistenzmechanismus, was das PFS verlängern sollte.
Tut es auch, wie die beim ASCO vorgestellte COMBI-d-Studie zeigte, die Dabrafenib mit dem MEK-Inhibitor Trametinib kombinierte. Allerdings fiel der Vorteil gegenüber Dabrafenib-Monotherapie beim PFS mit 9,3 versus 8,8 Monaten zwar signifikant, aber doch überschaubar aus.
"Das war etwas enttäuschend. Wir müssen jetzt nach weiteren Resistenzmechanismen suchen", so Keilholz. Möglich wäre auch, dass Patienten identifiziert werden können, die von der MEK-Inhibition besonders profitieren. "Viel mehr Personalisierung", das scheint beim Melanom das Gebot der Stunde zu sein.
So richtig komplex wird es, wenn nicht nur Gene, sondern auch funktionelle Parameter betrachtet werden. Transkriptom, Metabolom und Proteom lauten die Stichworte.
Wer diese Faktoren und ihren Einfluss auf Therapien untersuchen möchte, muss nicht nur das Tumorgenom, sondern auch noch freie Nukleinsäuren, DNA-Methylierungen, zirkulierende Tumorzellen und Krebsstammzellen berücksichtigen. In dem von der EU und dem europäischen Pharmaverband EFPIA mit 34 Millionen Euro geförderten OncoTrack-Projekt wird derzeit unter Beteiligung von neun Forschungszentren und.
Universitäten versucht, zumindest etwas mehr Licht in dieses noch weitgehend unerforschte Dunkel zu bringen. Schon jetzt ist klar: Einfacher wird die personalisierte Krebsmedizin dadurch auch nicht.
*) FOLFIRI: Folinsäure, 5-Fluorouracil, Irinotecan **) FOLFOX: Folinsäure, 5-Fluorouracil, Oxaliplatin