ATMP & Orphan Diseases: Datenquellen jenseits von RCT
ATMP und Orphan Drugs im AMNOG-Verfahren
Für Arzneimittel für neuartige Therapien (ATMP) und Orphan Drugs liegt zum Zeitpunkt der Nutzenbewertung häufig limitierte vergleichende Evidenz vor. Oftmals wird dies durch komplexe Therapieansätze und die kleinen Patientengruppen begründet. Hierdurch gehe die Planung und Durchführung von randomisierten kontrollierten Studien mit entsprechenden Herausforderungen einher.
Veröffentlicht:
Der G-BA hat nach Paragraf 35a Absatz 3b SGB V die Möglichkeit, die Erhebung von anwendungsbegleitenden Daten und von Auswertungen vom pharmazeutischen Unternehmer einzufordern.
© Sascha Steinach / ZB / picture alliance
Definition von Arzneimittel für neuartige Therapien (ATMP) und Orphan Drugs
ATMP lassen sich in drei Produktkategorien einteilen:1
Gentherapeutika, bei denen die therapeutische, prophylaktische oder diagnostische Wirkung auf dem Einbringen rekombinanter Gene in den Körper basiert.
Somatische Zelltherapeutika, die sich durch manipulierte Zellen oder Gewebe auszeichnen, deren biologische Eigenschaften verändert wurden, oder durch Zellen oder Gewebe, die nicht für die gleichen wesentlichen Funktionen im Körper vorgesehen sind.
Biotechnologisch bearbeitete Gewebeprodukte, die veränderte Zellen oder Gewebe zur Reparatur, Regeneration oder zum Ersatz von menschlichem Gewebe enthalten.
Bisher wurden nach Empfehlung durch die Europäische Arzneimittelagentur (EMA) überwiegend Gentherapeutika im Bereich der Hämatologie und Hämato-Onkologie zugelassen und nach Markteintritt in Deutschland im Rahmen der Nutzenbewertung bewertet (z. B. CAR-T-Zelltherapien zur Behandlung von Lymphomen und weitere Gentherapien zur Behandlung der Hämophilie, Sichelzellkrankheit und ß-Thalassämie). Neuere Zulassungen von Gentherapien betreffen auch weitere Indikationen mit bisher limitierten Behandlungsoptionen wie Epidermolysis bullosa (DEB).2
Die Zulassung von ATMP ist häufig mit der Vergabe eines Orphan-Drug-Status verbunden. Orphan Drugs sind Produkte, die zur Behandlung, Vorbeugung oder Diagnose einer lebensbedrohlichen oder chronisch belastenden Krankheit bestimmt sind, wobei die Prävalenz der Erkrankung in der Europäischen Union (EU) nicht höher als 5 von 10.000 betragen darf. Darüber hinaus darf für die Indikation keine zufriedenstellende Methode zur Diagnose, Prävention oder Behandlung der betreffenden Erkrankung zugelassen sein oder das Arzneimittel muss, falls eine solche Methode existiert, für die von der Erkrankung Betroffenen einen erheblichen Nutzen im Vergleich zu den bestehenden Behandlungsoptionen haben.3
Für die Feststellung des erheblichen Nutzens gegenüber bestehenden Behandlungsoptionen werden Kriterien herangezogen, die über die in der Arzneimittel-Nutzenverordnung (AMNutzenV) festgelegten Kriterien für die Feststellung eines Zusatznutzens in der Nutzenbewertung hinausgehen. So bezieht die EMA zusätzlich zur verbesserten Wirksamkeit und Verträglichkeit auch einen bedeutenden Beitrag zur Behandlung der Patientinnen und Patienten in Form einer erleichterten Selbstmedikation oder einer Verbesserung für die Compliance mit ein. Zudem muss für die Feststellung einer verbesserten Wirksamkeit und Verträglichkeit nicht zwingend ein quantitatives Element vorhanden sein, sondern diese kann sich auch auf die qualitative Beurteilung anhand klinischer Erfahrung stützen.4,5
Status quo der Regelungen zu ATMP und Orphan Drugs in der Nutzenbewertung
Da sowohl ATMP als auch Orphan Drugs zentral durch die Europäische Kommission zugelassen werden, unterliegen diese Produkte in der Regel der Nutzenbewertung nach Paragraf 35a SGB V. Für Gentherapien und somatische Zelltherapien besteht nach Paragraf 35a Absatz 1b SGB V die Verpflichtung zur Vorlage von Nachweisen für die Nutzenbewertung. Für biotechnologisch bearbeitete Gewebeprodukte ist weiterhin zu prüfen, ob diese in den Bereich der Bewertung von Untersuchungs- und Behandlungsmethoden nach den Paragrafen 135, 137c oder 137h SGB V fallen. Zumeist werden biotechnologisch bearbeitete Gewebeprodukte ebenfalls dem Regelungsbereich des Paragrafen 35a SGB V zugeordnet.
In Bezug auf die Bewertungsmaßstäbe bestehen für die Produktklasse der ATMP keine Sonderregelungen in der Nutzenbewertung. So sind für ATMP gleichermaßen Nachweise zum medizinischen Zusatznutzen im Verhältnis zu einer zweckmäßigen Vergleichstherapie vorzulegen.
Besteht für ein ATMP gleichzeitig ein Orphan-Drug-Status, dann greifen die in Paragraf 35a Absatz 1 Satz 11 SGB V definierten Sonderregelungen. Hiernach gilt der medizinische Zusatznutzen durch die Zulassung als belegt und Nachweise gegenüber einer zweckmäßigen Vergleichstherapie müssen nicht vorgelegt werden. Übersteigt der Umsatz eines Orphan Drugs mit der gesetzlichen Krankenversicherung innerhalb von zwölf Kalendermonaten einen Betrag von 30 Millionen Euro, entfällt diese Privilegierung und der pharmazeutische Unternehmer muss im Rahmen einer erneuten Nutzenbewertung Nachweise zum medizinischen Zusatznutzen gegenüber einer zweckmäßigen Vergleichstherapie vorlegen.
Da Orphan Drugs anwendungsgebietsbezogen ein Marktexklusivitätsrecht erhalten können, führt der G-BA Nutzenbewertungen dann nur in denjenigen Anwendungsgebieten von Orphan Drugs durch, in denen weiterhin aktive Schutzrechte in Form des Unterlagenschutzes und/oder der Marktexklusivität bestehen.6
Seit dem 12. Januar 2025 ist die EU-Verordnung (EU) 2021/2282 über die gemeinsame Bewertung von Gesundheitstechnologien auf EU-Ebene in Kraft. Als erste Produkte werden onkologische Arzneimittel und ATMP bewertet, auch dann, wenn für diese Arzneimittel ein Orphan-Drug-Status besteht. Ab Januar 2028 wird der Bewertungsrahmen auf alle weiteren Orphan Drugs ausgeweitet.7
Der G-BA wirkt als Mitglied der HTA-Koordinierungsgruppe und der dazugehörigen Subgruppen an der Erstellung der Joint Clinical Assessments (JCA) mit. Das Verfahren beginnt mit Validierung des Zulassungsantrages durch die EMA. Daraufhin wird der Bewertungsumfang (PICO-Fragestellung) für das jeweilige Arzneimittel zwischen den Mitgliedsstaaten abgestimmt und an den pharmazeutischen Unternehmer für die Dossiererstellung übermittelt. Der G-BA meldet hierfür den aus deutscher Sicht relevanten Bewertungsumfang zurück. Da für Orphan Drugs auf EU-Ebene keine Ausnahmeregelungen bestehen, wird dementsprechend auch in diesen Fällen ein Komparator, der unter Berücksichtigung des nationalen Versorgungskontextes einen geeigneten Vergleichsmaßstab darstellt, durch den G-BA festgelegt und gemeldet.
Ergebnisse der Nutzenbewertungen zu Orphan Drugs und ATMP
Orphan Drugs und meist auch ATMP werden für Anwendungsbereiche mit verhältnismäßig niedrigen Patientenzahlen entwickelt. Deshalb wird in den zugehörigen Nutzenbewertungsbeschlüssen überwiegend eine Anzahl von Patientinnen und Patienten in der gesetzlichen Krankenversicherung von unter 1.000 Patientinnen und Patienten ausgewiesen, in etwa einem Drittel sogar unter 100 Patientinnen und Patienten. Gleichzeitig stellen insbesondere ATMP komplexe Therapieansätze dar, die häufig auf der genetischen Manipulation patientenindividueller Zellen basieren.
Dies führt zu entsprechenden Herausforderungen beim Studiendesign randomisierter kontrollierter Studien (RCT) beispielsweise in Bezug auf die Möglichkeit der Verblindung oder geeigneter Erhebungsstrukturen zur Erfassung patientenberichteter Endpunkte. Werden diese Produkte für Behandlungssituationen mit fehlenden kausalen Therapiemöglichkeiten entwickelt, kann sich ggf. aus ethischen Gesichtspunkten zudem eine Rekrutierung von Patientinnen und Patienten in einen Vergleichsarm mit ausschließlich Best-Supportive-Care als Therapieoption als schwierig gestalten.
Dies führt dazu, dass für diese Arzneimittel die Zulassung häufig allein auf einarmigen Studien basiert und für eine vergleichende Nutzenbewertung indirekte bzw. historische Vergleiche erforderlich werden. Die Einreichung solcher nicht-randomisierten Vergleiche ist in der Nutzenbewertung regelhaft möglich und diese werden folglich durch das IQWiG bzw. den G-BA bewertet. Es ist jedoch festzustellen, dass sich aufgrund der Verwendung ungeeigneter Datenquellen oder einer nicht validen Methodik in den meisten Fällen keine hinreichend sicheren Schlussfolgerungen für die Nutzenbewertung aus den vorgelegten nicht-randomisierten Vergleichen ziehen lassen.
Schwierigkeiten ergeben sich, wenn die verglichenen Patientengruppen sich in ihren Patientencharakteristika wesentlich unterscheiden, die Daten aus dem verwendeten Register nicht geeignet sind, um die Fragestellung der Nutzenbewertung zu beantworten, oder die im Dossier dargestellte Methodik inadäquat oder nicht nachvollziehbar ist.
Indikationsspezifische Register stellen eine wichtige Datenquelle für die Durchführung nicht-randomisierter bzw. historischer Vergleiche dar. Bestehende Register wurden jedoch häufig ohne Berücksichtigung der Anforderungen, die für die Beantwortung der Fragestellung der Nutzenbewertung erforderlich wären, aufgesetzt. So fehlt in vielen Fällen eine systematische Identifikation von potenziellen Confoundern im Anwendungsgebiet und es findet dadurch keine Erhebung aller erforderlichen Baseline-Charakteristika durch den festgelegten Datensatz statt, oder die Daten werden zu unregelmäßig gemeldet, oder die Definition der Endpunkte ist im Vergleich zu den klinischen Studien nicht einheitlich oder es liegt eine hohe Anzahl von fehlenden Werten im Datensatz vor.
Weiterentwicklungen im allgemein anerkannten Stand der medizinischen Erkenntnisse in Bezug auf neue Tumormarker und prognostische Faktoren, die bislang in der Routineversorgung nicht erhoben wurden, können zusätzlich die Verwendung retrospektiver Daten aus indikationsspezifischen Registern erschweren. Für viele seltene Erkrankungen fehlt es zudem grundlegend an den erforderlichen Datenerhebungen in einem Medizinregister, um entsprechende Daten für die Nutzenbewertung vorlegen zu können.
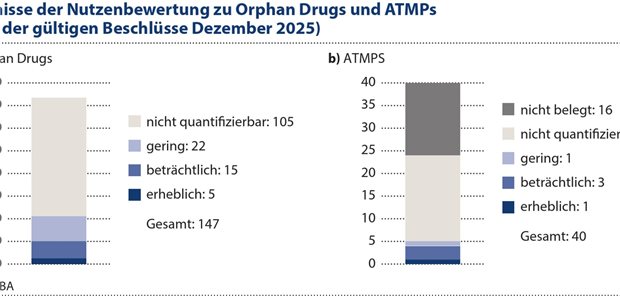
© Springer Medizin Verlag
Voraussetzung ist, dass diese Daten auch für die Fragestellung der Nutzenbewertung geeignet sind und in einer hinreichenden Datenqualität erhoben werden sowie eine adäquate statistische Methodik zur Auswertung des nicht-randomisierten Vergleiches eingesetzt wird. Dafür ist eine frühzeitige und präspezifizierte Planung durch den pharmazeutischen Unternehmer unter Erstellung eines Studienprotokolls und statistischen Analyseplans notwendig.
Zudem muss bei der Auswahl der Datenquelle berücksichtigt werden, dass für das zu betrachtende Anwendungsgebiet alle erforderlichen Angaben, die im Rahmen der Routineversorgung erhoben werden können, dokumentiert werden. Ist dies nicht der Fall, sollten entsprechende Datenfelder in der Datenquelle ergänzt werden. Da sich insbesondere in denjenigen Therapiesituationen ohne eine kausale Behandlungsmöglichkeit die prospektive Generierung versorgungsnaher Vergleichsdaten bzw. Daten zum natürlichen Krankheitsverlauf nach Inverkehrbringen des neuen Arzneimittels schwierig gestaltet, sollte die Datenerhebung im Register optimalerweise bereits parallel zur Durchführung der klinischen Studie bzw. vor Inverkehrbringen des Arzneimittels initiiert werden.
Darüber hinaus ist für die Nutzenbewertung grundsätzlich auch die Vorlage von Daten aus alternativen Studiendesigns (z. B. Plattform-Studien) möglich, die eine vergleichende Beurteilung der Therapieeffekte zulassen. Um eine verbesserte Nutzung und Aussagekraft von Daten aus Medizinregistern oder von Daten aus alternativen Studiendesigns für die Nutzenbewertung zu ermöglichen, sind jedoch auch entsprechende Investitionen zur Förderung des Aufbaus geeigneter Registerstrukturen und in den Ausbau der Forschungsdateninfrastruktur in Deutschland notwendig.
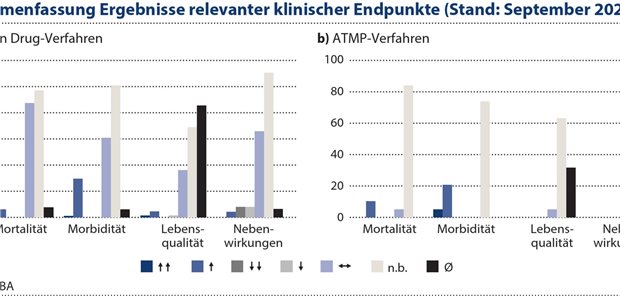
© Springer Medizin Verlag
Zudem werden über 50 Prozent der Orphan Drugs in Anwendungsgebieten mit einer Prävalenz von über 1 in 10.000 entwickelt, wogegen 96 Prozent der seltenen Erkrankungen eine Prävalenz von unter 1 in 10.000 aufweisen.9 Das Argument fehlender Behandlungsalternativen, die aus ethischen Erwägungen ein vergleichendes Studiendesign nicht ermöglichen, oder zu wenigen Patientinnen und Patienten im Anwendungsgebiet für eine ausreichende Rekrutierung greift daher für den Großteil der derzeit entwickelten Orphan Drugs nicht.
Darüber hinaus zeigen diverse Beispiele aus den Verfahren nach Paragraf 35a SGB V, dass auch in Anwendungsgebieten mit niedrigen Patientenzahlen (z. B. < 100 Patientinnen und Patienten) eine valide RCT realisierbar ist und für die Nutzenbewertung herangezogen werden kann.10,11,12 Auch komplexe Therapieansätze wie eine CAR-T-Zelltherapie sprechen nicht grundsätzlich gegen die Durchführung einer vergleichenden klinischen Studie wie aus verschiedenen Nutzenbewertungsverfahren zu frühen Therapielinien des DLBCL und multiplen Myeloms ersichtlich ist.13,14,15,16
Unbestritten ist, dass sich für Ultra-Orphan-Indikationen mit einer Prävalenz von <1 in 50 000 Fallgestaltungen ergeben können, in denen aufgrund der sehr kleinen Patientenzahlen keine RCT machbar ist.
Rolle der anwendungsbegleitenden Datenerhebung (AbD)
Der G-BA hat nach Paragraf 35a Absatz 3b SGB V die Möglichkeit, die Erhebung von anwendungsbegleitenden Daten und von Auswertungen vom pharmazeutischen Unternehmer einzufordern. Die Möglichkeit der Forderung beschränkt sich auf Arzneimittel mit einem Orphan Drug-Status oder auf Arzneimittel, die eine bedingte Zulassung oder eine Zulassung unter außergewöhnlichen Umständen erhalten.
Der G-BA kann die Befugnis zur Versorgung mit einem Arzneimittel, für das eine solche Datenerhebung gefordert wurde, auf diejenigen Leistungserbringer beschränken, die an der Datenerhebung teilnehmen. Darüber hinaus muss der G-BA Vorgaben an die Dauer, die Art und den Umfang der Datenerhebung und die Auswertung machen, inklusive zur Methodik und zu patientenrelevanten Endpunkten und deren Erfassung.
Derzeit laufen fünf anwendungsbegleitende Studien, von denen vier ATMP betreffen (Onasemnogen Aberparvovec (spinale Muskelatrophie), Brexucabtagen Autoleucel (Mantelzelllymphom), Etranacogen Dezaparvovec (Hämophilie B), Valoctocogen Roxaparvovec (Hämophilie A)). Die erste Nutzenbewertung auf der Grundlage einer anwendungsbegleitenden Datenerhebung wird voraussichtlich Mitte 2027 für den Wirkstoff Onasemnogen Aberparvovec erfolgen, sieben Jahre, nachdem der Wirkstoff in Verkehr gekommen ist.
Die anwendungsbegleitende Datenerhebung stellt aufgrund der bestehenden Herausforderungen in den Registerstrukturen in Deutschland kein geeignetes Instrument dar, um Evidenzlücken für Orphan Drugs und ATMP in der Nutzenbewertung zeitnah zu schließen. So kann der Beschluss zur Forderung einer AbD erst mit Markteintritt des betroffenen Arzneimittels seine Wirkung entfalten, wonach sich eine zeitaufwändige Abstimmung von Studienunterlagen mit dem pharmazeutischen Unternehmer anschließt.
Obwohl häufig umfassendere Änderungen an der Datenquelle zur Beantwortung der Fragestellung der Nutzenbewertung erforderlich sind, kann der G-BA dabei keine direkten Anforderungen an die Registerbetreiber selbst stellen, sondern nur an den jeweiligen pharmazeutischen Unternehmer. Dies verzögert wesentlich den Beginn der Datenerhebung. Durch die zusätzlich notwendige Studiendauer für eine ausreichende Beobachtungszeit der Endpunkte sind somit weitergehende Daten für die Nutzenbewertung oftmals erst mehrere Jahre nach Markteintritt verfügbar.
Aufgrund des nicht-randomisierten Charakters der Datenerhebung ist zudem eine ausreichende Patientenzahl für eine sachgerechte Adjustierung für potenzielle Effektmodifikatoren (Confounder) notwendig. Dies erfordert für die Realisierbarkeit der anwendungsbegleitenden Datenerhebung mindestens 100 Patientinnen und Patienten im Anwendungsgebiet. Daher ermöglicht das Instrument der anwendungsbegleitenden Datenerhebung auch in Bezug auf Ultra-Orphans keine weitergehende Schließung von Evidenzlücken.17
Fazit und Ausblick
Der Status als Orphan Drug oder als ATMP ist nicht gleichzusetzen mit der fehlenden Machbarkeit einer RCT. In spezifischen Behandlungskonstellationen, beispielsweise bei Fehlen kausaler Therapieansätze oder in Bezug auf sehr seltene Erkrankungen kann die Durchführung mit besonderen Herausforderungen verbunden und im Einzelfall aufgrund ethischer Erwägungen tatsächlich nicht möglich sein. Dies ist jedoch abzugrenzen von Therapiesituationen, in denen die Durchführung einer RCT zwar grundsätzlich möglich wäre, sich der pharmazeutische Unternehmer aber aufgrund der damit einhergehenden Herausforderungen aus strategischen oder wirtschaftlichen Gründen dagegen entscheidet. Dies führt dazu, dass eine Quantifizierung des Zusatznutzens in der Nutzenbewertung vor dem Hintergrund der einarmigen Studiendaten in der Regel nicht möglich ist.
Ein proaktiver Ausbau der Forschungsdateninfrastruktur inklusive indikationsspezifischer Registerstrukturen in Deutschland kann genutzt werden, um die Evidenzbasis von Orphan Drugs und ATMP zu verbessern und für die Nutzenbewertung zugänglich zu machen. Für eine effiziente und zeitnahe Schließung von Evidenzlücken müssen frühzeitig Datenstrukturen etabliert werden, um Vergleichsdaten bereits vor Markteintritt eines Arzneimittels zu erheben und Potenziale für die Durchführung neuer Studiendesigns zu eröffnen. Hierdurch kann auch in Indikationen, in denen bisher keine geeignete Behandlungsoption zur Verfügung stehen, ein methodisch geeigneter nicht-randomisierter Vergleich zu Daten zum natürlichen Krankheitsverlauf bzw. einer historischen Kohorte ermöglicht werden.

Dr. Rimma Berenstein
© Svea Pietschmann / G-BA
Literatur
1 https://www.ema.europa.eu/en/human-regulatory-overview/advanced-therapy-medicinal products-overview
2 https://www.ema.europa.eu/en/news/first-topical-gene-therapy-treatment-dystrophic-epidermolysis-bullosa
3 https://www.ema.europa.eu/en/human-regulatory-overview/orphan-designation-overview
4 Regulation (EC) No 141/2000 of the European Parliament and of the Council of 16 December 1999 on orphan medicinal products, OJ L 18, 22.1.2000; https://eur-lex.europa.eu/eli/reg/2000/141/oj/eng
5 Commission Regulation (EC) No 847/2000 of 27 April 2000 laying down the provisions for implementation of the criteria for designation of a medicinal product as an orphan medicinal product and definitions of the concepts ‚similar medicinal product‘ and ‚clinical superiority‘ OJ L 103, 28.4.2000; https://eur-lex.europa.eu/eli/reg/2000/847/oj/eng
6 G-BA Beschluss, 20. November 2025, Verfahrensordnung, Änderung zum 5. Kapitel – Änderungen aus Anlass der Ersten Verordnung zur Änderung der Arzneimittel-Nutzenbewertungsverordnung – Unterlagenschutz, https://www.g-ba.de/beschluesse/7546/
7 Regulation (EU) 2021/2282 of the European Parliament and of the Council of 15 December 2021 on health technology assessment and amending Directive 2011/24/EU (Text with EEA relevance); PE/80/2021/INIT; OJ L 458, 22.12.2021; https://eur-lex.europa.eu/legal-content/EN/TXT/?uri=CELEX:32021R2282
8 Commission Staff Working Document Evaluation Joint evaluation of Regulation (EC) No 1901/2006 of the European Parliament and of the Council of 12 December 2006 on medicinal products for paediatric use and Regulation (EC) No 141/2000 of the European Parliament and of the Council of 16 December 1999 on orphan medicinal products SWD/2020/0163 final; https://eur-lex.europa.eu/legal-content/EN/TXT/?uri=CELEX%3A52020SC0163
9 Aartsma-Rus A., Dooms M. , Le Cam Y., 2021, Orphan Medicine Incentives: How to Address the Unmet Needs of Rare Disease Patients by Optimizing the European Orphan Medicinal Product Landscape Guiding Principles and Policy Proposals by the European Expert Group for Orphan Drug Incentives (OD Expert Group), Frontiers in Pharmacology, Volume 12 – 2021, https://www.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2021.744532
10 G-BA Beschluss zu Tivozanib, 19. April 2018, https://www.g-ba.de/bewertungsverfahren/nutzenbewertung/324/#beschluesse
11 G-BA Beschluss zu Blinatumomab, 20. Januar 2022, https://www.g-ba.de/bewertungsverfahren/nutzenbewertung/720/#beschluesse
12 G-BA Beschluss zu Axitinib, 21. September 2017, https://www.g-ba.de/bewertungsverfahren/nutzenbewertung/283/#beschluesse
13 G-BA Beschluss zu Axicabtagen-Ciloleucel, 21. Dezember 2023, https://www.g-ba.de/bewertungsverfahren/nutzenbewertung/901/#beschluesse
14 G-BA Beschluss zu Lisocabtagen Maraleucel, 16. November 2023, https://www.g-ba.de/bewertungsverfahren/nutzenbewertung/960/#beschluesse
15G-BA Beschluss zu Ciltacabtagen Autoleucel, 15. Mai 2025, https://www.g-ba.de/bewertungsverfahren/nutzenbewertung/1088/#beschluesse
16 G-BA Beschluss zu Idecabtagen Vicleucel, 19. Dezember 2024, https://www.g-ba.de/bewertungsverfahren/nutzenbewertung/1068/#beschluesse
17 IQWIG, 14. Mai 2020, [A19-43] Wissenschaftliche Ausarbeitung von Konzepten zur Generierung versorgungsnaher Daten und deren Auswertung zum Zwecke der Nutzenbewertung von Arzneimitteln nach § 35a SGB V - Rapid Report, https://www.iqwig.de/projekte/a19-43.html