ATMP & Orphan Diseases: Datenquellen jenseits von RCT
Die Anwendungsbegleitende Datenerhebung (AbD): Eine kritische Bestandsaufnahme
Mit dem GSAV wurde die AbD für Arzneimittel mit schwacher Zulassungsevidenz eingeführt. Insbesondere für Orphan Drugs sollte durch nachgelagerte Datenerhebungen eine bessere Grundlage für eine erneute Nutzenbewertung geschaffen werden. Seit 2020 wurden jedoch nur fünf AbD-Verfahren umgesetzt. Die erwartete Verbesserung der Evidenz ist unrealistisch und das Potenzial für Kostensenkungen gering.
Veröffentlicht:
Nach fünf Jahren Verfahrenspraxis zeigt sich, dass die Realisierbarkeit und Angemessenheit einer AbD in vielen Fällen bereits im Vorfeld infrage gestellt werden kann.
© janews094 / stock.adobe.com
Am 16. August 2019 trat das Gesetz für mehr Sicherheit in der Arzneimittelversorgung (GSAV) in Kraft. Es wurde mit Paragraf 35a Abs. 3b SGB V eine Ergänzung vorgenommen, die es dem Gemeinsamen Bundesausschuss (G-BA) ermöglicht, bei Arzneimitteln zur Behandlung eines seltenen Leidens (Orphan Drug), Arzneimitteln mit einer bedingten Genehmigung für das Inverkehrbringen (Conditional Marketing Authorisation, CMA) sowie Arzneimitteln mit einer Zulassung unter außergewöhnlichen Umständen (Marketing Authorisation under Exceptional Circumstances, MAEC) die Vorlage anwendungsbegleitender Datenerhebungen (AbD) zum Zweck einer (erneuten) Nutzenbewertung zu fordern. Der Schwerpunkt liegt dabei auf Anwendungsbeobachtungen, Fall-Kontroll-Studien und Registerstudien. Randomisierte kontrollierte Studien (RCT) sind ausgeschlossen.1
Sollte nach der Durchführung einer AbD der Zusatznutzen eines Orphan Drugs anhand der gewonnenen Daten weiterhin nicht quantifizierbar sein, ermöglicht es dem GKV-Spitzenverband (GKV-SV) eine weitere Neuregelung in Paragraf 130b Abs. 3 SGB V einen Abschlag auf den im Rahmen der Erstbewertung verhandelten Erstattungsbetrag zu vereinbaren. Bei einer alleinigen CMA oder MAEC finden ebenfalls erneute Preisverhandlungen statt.
Um möglichst vollständige und valide Daten aus der Versorgung von Versicherten zu erfassen, kann der G-BA die Befugnis zur Verordnung der betroffenen Arzneimittel zu Lasten der GKV auf solche Leistungserbringer beschränken, die an der geforderten AbD mitwirken.
Der Gesetzgeber formulierte folgende Ziele, die er mit dieser Gesetzesanpassung erreichen wollte:
1. Arzneimittel, die eine Zulassung auf Basis von schwacher Evidenz zugesprochen bekommen haben, insbesondere Orphan Drugs, sollen den Patientinnen und Patienten in der GKV (weiterhin) zügig zur Verfügung stehen und gleichzeitig soll eine bessere Datenbasis zur (erneuten) Bewertung des Zusatznutzens geschaffen werden.
2. Es soll ein Anreiz geschaffen werden, AbDs durchzuführen und gleichzeitig vermieden werden, dass der Erstattungsbetrag dauerhaft gleich hoch bleibt, obwohl keine hinreichenden Belege für einen Zusatznutzen vorhanden sind.1 Somit ist die AbD sowohl als Instrument zur Schaffung einer besseren Evidenzgrundlage als auch als Instrument zur Preisregulierung aufzufassen.
Da die Zusatznutzenfiktion für Orphan Drugs in Paragraf 35a Abs. 1 Satz 11 eine Ausnahme von der regulären Nutzenbewertung darstellt, kann die AbD zudem als korrigierende Sonderregelung innerhalb dieser Ausnahme angesehen werden.
Zwischenstand des AbD-Verfahrens beim G-BA
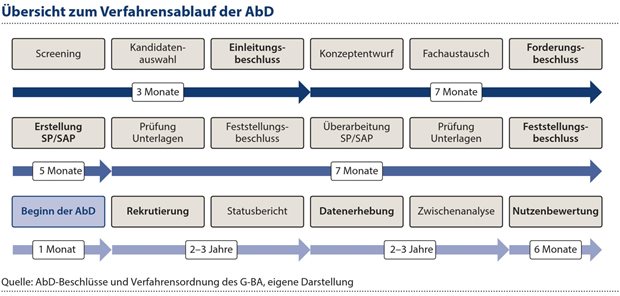
Seit März 2020 prüft der G-BA laufende Zulassungsverfahren bei der Europäischen Arzneimittel-Agentur (EMA) im Hinblick auf die Eignung der jeweiligen Arzneimittel für eine AbD unter Berücksichtigung der gesetzlichen Vorgaben. Für ein erstes Screening werden üblicherweise öffentlich zugängliche Informationen aus den Zulassungsverfahren und aus Studienregistern herangezogen. Liegen im Rahmen eines Zulassungsverfahrens keine RCT-Daten vor, wird üblicherweise davon ausgegangen, dass eine ausreichende Evidenzgrundlage für eine spätere Nutzenbewertung nicht gegeben ist.2Es wurden im Zeitraum von März 2020 bis März 2025 auf der Grundlage von 262 monitorierten Wirkstoffen insgesamt 69 Zulassungsverfahren für Arzneimittel mit Orphan Designation und/oder möglicher CMA/MAEC identifiziert, die auf Basis von einarmigen klinischen Studien erfolgten, so dass grundsätzlich von der Erforderlichkeit einer AbD auszugehen war (siehe Abb. 1). Diese bildeten den Pool der vom G-BA zu beratenden möglichen AbD-Kandidaten.
Die Auswahl ist eine Einzelfallentscheidung und erfolgt laut Paragraf 54 Abs. 2 VerfO unter Berücksichtigung der Realisierbarkeit und Angemessenheit einer Datenerhebung. Dazu kann eine Recherche nach verfügbaren Registern im Anwendungsgebiet (AWG) durchgeführt werden. Ebenfalls wird versucht, einzuschätzen, ob ein AWG mit besonders geringer Patientenzahl vorliegt. Man orientiert sich dabei an einer vom IQWiG vorgeschlagenen Grenze von 100 Patientinnen und Patienten, ab der ein adjustierter indirekter Vergleich methodisch sinnvoll durchführbar ist.3,4
Eine zweckmäßige Vergleichstherapie (zVT) wird ebenfalls bestimmt, welche die Grundlage für die Diskussionen zu möglichen Komparatoren bildet. Wirkstoffkandidaten in AWGs ohne verfügbare Therapiealternative werden üblicherweise nicht weiterverfolgt.
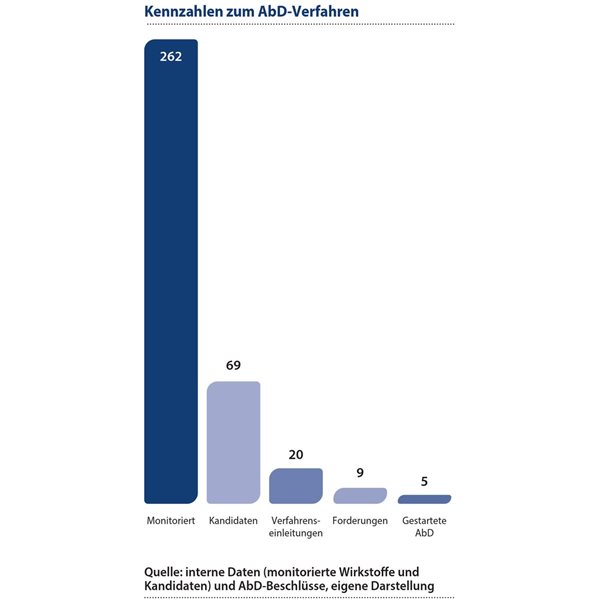
© Springer Medizin Verlag
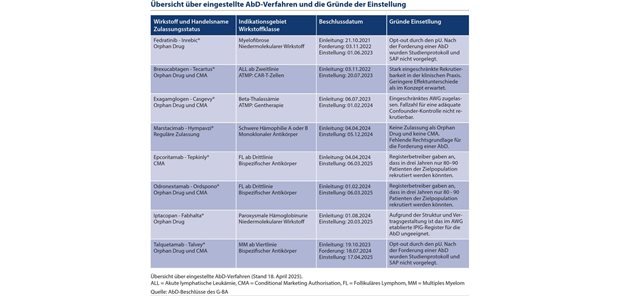
Auf Basis von 69 Kandidaten wurden bislang 20 AbD-Verfahren eingeleitet. Von diesen wiederum konnte für neun Wirkstoffe eine AbD gefordert werden. Nach einem Forderungsbeschluss wurden zwei AbD-Verfahren wieder eingestellt, da die pUs ihrer Pflicht zur Erstellung eines Studienprotokolls (SP) und eines Statistischen Analyseplans (SAP) nicht nachkamen. Einmal führte der Verlust der Rechtsgrundlage mit der Zulassung zu einer Verfahrenseinstellung (siehe Abb. 1, Tab. 1, Tab. 2 ). Für acht Arzneimittel mit Verfahrenseinleitung liefen parallel RCTs in früheren Therapielinien. Davon wurden sieben Arzneimittel mit einer CMA in Verkehr gebracht.
Bis zum 20. März 2025, etwa sechs Jahre nach Inkrafttreten des GSAV, sind lediglich fünf AbDs gestartet und erheben Daten aus der praktischen Anwendung der jeweiligen Arzneimittel in Deutschland.
© Springer Medizin Verlag
Evidenzlage und AbD-Potenzial von Orphan Drugs im AMNOG-Verfahren
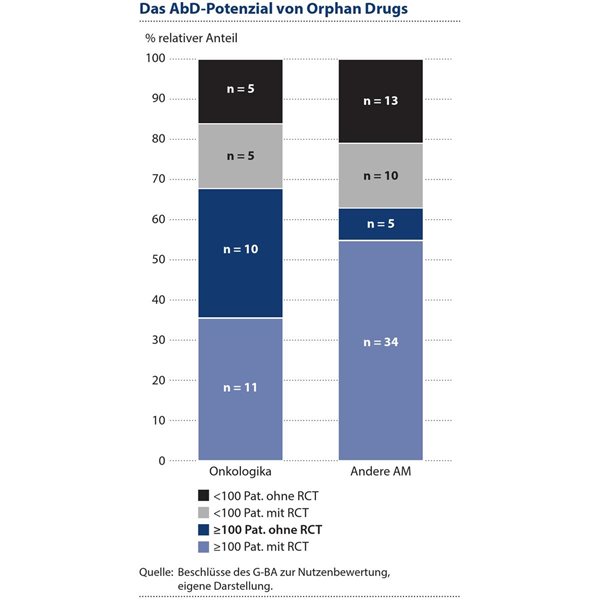
In der auf den Internetseiten des G-BA zugänglichen AMNOG-Datenbank konnten insgesamt 217 Nutzenbewertungen für Orphan Drugs identifiziert werden, deren Einleitung in den Jahren 2020 bis 2024 erfolgte. Berücksichtigt wurden jene Verfahren, bei denen der G-BA im Rahmen der gesetzlichen Zusatznutzenfiktion die Dossierbewertung durchführte und für die bis zum 20. März 2025 erstmals ein Beschluss vorlag. Diese Auswahl bildet die Evidenzbasis zu Beginn der Verfügbarkeit in Deutschland gut ab und umfasste insbesondere auch Orphan Drugs, für welche die Durchführung einer AbD diskutiert werden konnte. Eingeschlossen wurden in die vorliegende Betrachtung 93 Bewertungsverfahren. Es wurden dabei 31 Verfahren für Onkologika und 62 Verfahren in nicht-onkologischen AWGs durchgeführt.
Insgesamt lagen für 60 von 93 Verfahren Daten aus RCTs vor. In nicht-onkologischen AWGs wurden dabei häufiger RCTs durchgeführt als in onkologischen AWGs. Der Zusatznutzen konnte auf Basis einer vorliegenden RCT jedoch lediglich in 26 von 60 Fällen quantifiziert werden. In weiteren elf Verfahren mit RCT konnte zumindest auf Endpunktebene ein Vorteil vom G-BA abgeleitet werden, in drei Verfahren zeigten sich jedoch ausschließlich Nachteile. Insgesamt konnte der Zusatznutzen in 66 von 93 Fällen nicht quantifiziert werden. Dabei lagen für 33 Verfahren keine für die Nutzenbewertung verwertbaren Daten vor. In 52 von 93 Verfahren wurde der Zusatznutzen alleinig auf Basis der gesetzlichen Zusatznutzenfiktion festgestellt. In nur einem Verfahren konnte der Zusatznutzen ohne RCT quantifiziert werden (Atidarsagen autotemcel).
Laut den veröffentlichten Beschlussdokumenten lag bei 33 Verfahren eine besonders geringe Populationsgröße von unter 100 Patientinnen und Patienten vor. Es wurde dabei die untere Spanne der angegebenen Patientenzahl betrachtet, um unter Berücksichtigung von Unsicherheiten, AWGs mit sehr kleinen Populationsgrößen sicher erfassen zu können. Bei AWGs mit mehreren Teilpopulationen wurden die Patientenzahlen im Rahmen der Auswertung addiert.
Lediglich 15 der 93 bewerteten Orphan Drugs erfüllten zwei zentrale AbD-Kriterien: Es lag keine RCT als Bewertungsgrundlage vor und das AWG umfasste mehr als 100 Patientinnen und Patienten (siehe Abb. 3). In dieser Gruppe wurde für sechs Wirkstoffe ein AbD-Verfahren eingeleitet.
Grenzen der praktischen Umsetzung von AbD-Verfahren
Lange Verfahrensdauer
Ein Kernproblem der AbD stellt die lange Verfahrensdauer dar. Insbesondere in dynamischen Anwendungsgebieten ist zu befürchten, dass die Versorgungsrelevanz der erhobenen Daten zum Zeitpunkt der Nutzenbewertung nicht mehr gegeben ist.
Die EMA geht bei Zulassungsverfahren in onkologischen Indikationsgebieten häufig adaptiv vor. Ein Wirkstoff wird zunächst auf Basis erster klinischer Daten für ein begrenztes Patientenkollektiv mit hohem medizinischem Bedarf mit einer CMA zugelassen. Die Phase-III-RCT in einer früheren Therapielinie rekrutiert bereits und der Wirkstoff wird voraussichtlich mittelfristig in dieser neuen Behandlungssituation zugelassen und eingesetzt werden.5,6 Damit ergibt sich die Frage nach der zukünftigen Versorgungsrelevanz von Daten aus einer AbD, die ausschließlich das zunächst adaptiv zugelassene Anwendungsgebiet adressiert. Kritisch ist es, wenn die AbD unter Berücksichtigung bisher veranschlagter Verfahrensfristen erst dann abgeschlossen werden kann, wenn höherwertigere Evidenz in dieser früheren Therapielinie bereits absehbar vorliegt.
© Springer Medizin Verlag
Sehr große Effektunterschiede notwendig
Bei methodisch adäquat durchgeführten vergleichenden Studien ohne Randomisierung setzt das IQWiG voraus, dass Aussagen zum Nutzen oder Schaden einer Intervention erst dann möglich sind, wenn das 95%-Konfidenzintervall für einen beobachteten Effekt bei Endpunkten der Kategorie schwerwiegende/schwere Folgekomplikationen einen Schwellenwert von 2-5 für das relative Risiko überschreitet.7
Dies liegt zwar unterhalb der Schwelle eines dramatischen Effekts, die AbD ist unter der Voraussetzung einer verschobenen Nullhypothese jedoch absehbar nur ausreichend sensitiv, um sehr große Effektunterschiede bei patientenrelevanten Endpunkten nachweisen zu können. Davon ist umso weniger auszugehen, je wirksamer die als Komparator zur Verfügung stehenden Therapiealternativen sind.
Hier ergibt sich ein offensichtliches Dilemma, da die AbD gerade bei Arzneimitteln ohne hinreichende Belege für einen Zusatznutzen zu niedrigeren Erstattungsbeträgen führen soll. Eine klassische Fallzahlabschätzung, wie sie im Rahmen einer klinischen Studie zur Bestätigung einer Überlegenheitshypothese durchgeführt wird, stößt bei der AbD an Grenzen. Es bestehen zudem Zweifel, wie ein Behandlungseffekt mit notwendigen Abstufungen den laut Paragraf 5 Absatz 7 AM-NutzenV vorgegebenen Nutzenkategorien zugeordnet werden soll.
Selbst etablierte Register nur nach Anpassung nutzbar
Für die Umsetzung einer AbD ist es vorteilhaft, ein vorhandenes Register nutzen zu können, welches bereits patientenrelevante Endpunkte erhebt und einen wesentlichen Anteil der jeweiligen Zielpopulation erfasst. Bisher waren allerdings selbst etablierte krankheitsspezifische Register nur unter dem Vorbehalt noch durchzuführender Anpassungen als Datenquelle für eine AbD geeignet.
Das IQWiG kritisierte im Rahmen der Konzepterstellung wiederholt, dass patientenberichtete Endpunkte und unerwünschte Ereignisse nicht in ausreichendem Umfang erhoben werden, dass die Basisdaten relevante Störgrößen (Confounder) für indirekte Vergleiche nicht umfassten und dass die Maßnahmen zur Gewährleistung von Vollständigkeit und Richtigkeit der erfassten Daten (Source Data Verification) nicht ausreichten.8,9

© Springer Medizin Verlag
Hoher administrativer Aufwand
AbDs sind mit einem hohen administrativen Aufwand verbunden. Dies ist hauptsächlich auf die hohen Anforderungen an den Datenumfang und die Datenqualität zurückzuführen. Obwohl der Gesetzgeber festgelegt hat, dass die Datenerhebung anwendungsbegleitend erfolgen soll und keine Einschränkungen für die verordnenden Ärztinnen und Ärzte hinsichtlich der Arzneimittelversorgung bestehen (keine Randomisierung oder Studienvorgaben), muss die AbD dennoch zum Zweck der Nutzenbewertung durchgeführt werden.1
Insbesondere die Erhebung von patientenberichteten Endpunkten ist mit einem hohen personellen und logistischen Aufwand verbunden. Hierbei ist auch das enge zeitliche Toleranzfenster der Datenerfassung für den jeweiligen Patienten zu berücksichtigen.11,12 Zudem stellen die Anforderungen an die Source Data Verification Registerbetreiber und Leistungserbringer vor Herausforderungen.12
Da die auf Kosten des pUs generierten Daten bei der erneuten Nutzenbewertung laut Paragraf 7 Absatz 2a AM-NutzenV berücksichtigt werden müssen, ist eine umfangreiche Prüfung und Beratung der jeweiligen AbD-Projekte seitens des G-BA im Vorfeld erforderlich. Beim IQWiG werden wichtige Ressourcen durch die Konzepterstellung sowie die Abnahme von Studienprotokollen und statistischen Analyseplänen gebunden.
Wenn möglich, sollte für mehrere neue Arzneimittel im gleichen AWG eine gemeinsame AbD erfolgen. Die Datenerhebung über ein Masterprotokoll im selben Register oder derselben Plattformstudie mit gemeinsamer Kontrollgruppe kann Aufwand und Kosten senken.13 Bei einer AbD mit Versorgungsbeschränkung für mehrere Wirkstoffe im gleichen AWG hätte jedoch ein pU, der sich der AbD verweigert und stattdessen eine neue Erstattungsbetragsverhandlung mit dem GKV-SV anstrebt, einen Wettbewerbsvorteil gegenüber Mitbewerbern, die zusätzliche Evidenz generieren.
Überschätzung der verfügbaren Patientenzahl
Üblicherweise erfolgt eine Abschätzung der verfügbaren Patientenzahl durch das IQWiG im AbD-Konzept auf Basis öffentlich verfügbarer Informationen, insbesondere unter Berücksichtigung von bereits im Rahmen der Nutzenbewertung getroffener Beschlüsse. Die Berechnung von Populationsgrößen ist regelmäßig mit hohen Unsicherheiten verbunden. Ohne belastbare Daten zur erwartbaren Effektivität eines neuen Wirkstoffes in Bezug auf patientenrelevante Endpunkte gestaltete sich auch die Fallzahlabschätzung schwierig. Unklar ist zudem die zukünftige Nachfrage nach einem neuen Wirkstoff in der Versorgungspraxis.
Der Grund für drei Verfahrenseinstellungen in den Indikationsgebieten follikuläres Lymphom und akute lymphatische Leukämie war eine in der Praxis absehbar geringere rekrutierbare Patientenzahl, die nach Einschätzung der Fachexperten und Registerbetreiber deutlich unter der vom IQWiG bestimmten Patientenzahl lag.14,15
Schlussfolgerungen
Das AbD-Verfahren bleibt hinter den Erwartungen zurück. Der Gesetzgeber ging ursprünglich davon aus, dass etwa neun bis zehn AbDs pro Jahr vom G-BA gefordert und auch durchgeführt werden.1 Nach fünf Jahren Verfahrenspraxis zeigt sich vor allem, dass die Realisierbarkeit und Angemessenheit einer AbD in vielen Fällen bereits im Vorfeld infrage gestellt werden kann. Bereits in der Anfangsphase wurde das Verfahren lediglich als eine Notlösung im Einzelfall bewertet.16 Auch der Sachverständigenrat Gesundheit und Pflege (SVR) kommt in seinem Jahresgutachten 2025 zu dem Schluss, dass die AbD in ihrer derzeitigen Form als insgesamt dysfunktional anzusehen ist.17
© Springer Medizin Verlag
Qualitätsmängel innerhalb der vorgelegten RCTs können dazu führen, dass sich ein Zusatznutzen nicht quantifizieren lässt. Häufig zeigen sich aber auch keine Vorteile in den vom G-BA akzeptierten patientenrelevanten Endpunkten. Im Rahmen der Kandidatenauswahl kann vorab keine umfassende methodische und inhaltliche Prüfung der identifizierten Studien durchgeführt werden. Dies obliegt der anschließenden Nutzenbewertung.
Bestehende Evidenzlücken erst nach der Zulassung mit einer AbD zu schließen, ist mit hohen Hürden verbunden. In vielen Fällen ist es für ein Orphan Drug nach Marktverfügbarkeit nicht mehr möglich, die notwendige vergleichende Evidenz zur Quantifizierung des Zusatznutzens zu generieren, insbesondere in einem praktikablen Zeitrahmen und mit vertretbarem Aufwand. Insgesamt handelt es sich bei der AbD um ein komplexes Verfahren, das mit einem erheblichen Aufwand und Ressourceneinsatz verbunden ist, sowohl für den G-BA, die Registerbetreiber und die versorgungsbefugten Leistungserbringer, als auch das IQWiG.
Aufgrund der geringen Anzahl geeigneter Kandidaten ist das Potenzial für Kostensenkungen durch nachgelagerte AbDs im Vergleich zum gesamten AMNOG-Verfahren als marginal einzuschätzen. Angesichts der schnellen Innovationszyklen in der pharmazeutischen Industrie und der zugleich langwierigen Verfahren, erscheint zudem die Gewinnung versorgungsrelevanter Erkenntnisse häufig fraglich.
Ausblick und Vorschläge
RCTs bleiben auch zukünftig der Goldstandard im Rahmen der Zulassung und der Nutzenbewertung. Vorteile von RCTs bei seltenen Erkrankungen können darin bestehen, dass die benötigte Patientenzahl geringer sein kann als bei einer AbD, da keine Confounder-Adjustierung erforderlich ist. Zudem ist unter Berücksichtigung der Vorgaben des IQWiG eine RCT bei zu erwartenden geringen bis moderaten Effektstärken das geeignetere Instrument.Primäres Ziel sollte es daher sein, RCTs durchzuführen und die Qualität von geplanten RCTs zu verbessern, um diese nicht nur für den Zulassungsprozess, sondern auch für die Nutzenbewertung oder das EU-HTA-Verfahren verwenden zu können. Falls RCTs nicht durchführbar sind, empfiehlt es sich, vergleichende Daten zum natürlichen Verlauf der Erkrankung oder zum bisherigen Therapiestandard parallel zur Zulassungsstudie prospektiv zu erheben, um diese bereits für die Nutzenbewertung vorlegen zu können. Hierfür sollten etablierte Register gezielt angepasst und genutzt werden.
Für die EMA sind statistische Modelle und Tests, in denen Daten aus einarmigen Studien mit externen Kontrollen verglichen werden, nicht zum Nachweis der Wirksamkeit ausreichend, da weder Modellierungsverfahren noch Matchingansätze die Verzerrung ausreichend reduzieren könnten. Externe Daten aus Registern würden deshalb lediglich unterstützend herangezogen.18,19 Das Zulassungsverfahren setzt somit bislang keine ausreichenden Anreize, um in den Ausnahmesituationen, in denen einarmige Studiendaten zur Nutzen-Risiko-Abwägung akzeptiert werden, geeignete Daten für adjustierte indirekte Vergleiche bereits vorab zu erheben.
Orphan Drugs werden schon in der ersten Umsetzungsstufe des EU-HTA-Verfahrens erfasst, wenn es sich um Onkologika oder ATMPs handelt.20 Das EU-HTA-Verfahren ist grundsätzlich als vergleichende Bewertung angelegt. Im Rahmen des Scoping-Prozesses wird auch für ein Orphan Drug ein vollständiges PICO mit einem Komparator zur Festlegung des Bewertungsumfanges erstellt.21 Es bietet sich somit an, über den zukünftigen Umgang mit Orphan-Drugs im nachgelagerten nationalen AMNOG-Verfahren erneut zu diskutieren.
Im Sinne einer Vereinheitlichung des Vorgehens wäre es nur konsequent, die Nutzenbewertung aller Arzneimittel mit neuen Wirkstoffen unabhängig vom Orphan-Drug-Status gegenüber einer zVT transparent durchzuführen. Ebenfalls konsequent wäre es, auch für Orphan Drugs fehlende Evidenz frühzeitig über einen reduzierten Erstattungsbetrag zu berücksichtigen, da sich die als korrigierende Sonderregelung zur Zusatznutzenfiktion konzipierte AbD als nicht praxistauglich erwiesen hat. Anreize für ein zügiges Inverkehrbringen bleiben grundsätzlich sinnvoll und könnten ebenfalls auf der Ebene der Vereinbarungen über Erstattungsbeträge in Paragraf 130 b SGB V verankert werden. Diese sollten jedoch gezielt auf solche Orphan Drugs fokussiert werden, die einen hohen medizinischen Bedarf adressieren oder aufgrund einer besonders geringen Patientenzahl Herausforderungen in der Evidenzgenerierung aufweisen.
Das AbD-Verfahren sollte hingegen perspektivisch eingestellt werden, da die vom Gesetzgeber angestrebten Ziele in der Praxis nicht erreicht werden können. Weder lassen sich durch AbDs systemrelevante Einsparungen erzielen, noch kann auf diesem Wege die zum Zeitpunkt der Zulassung von Orphan Drugs bestehende unzureichende Evidenzlage zeitnah und umfassend verbessert werden. Die im Rahmen der AbD bisher gewonnenen methodischen Erkenntnisse und Erfahrungen sollten vielmehr genutzt werden, um Studienplanungen für zukünftige Zulassungsverfahren und HTA-Prozesse zu optimieren sowie die Qualität der Registerlandschaft in Deutschland nachhaltig zu stärken.
Die im Rahmen des Referates präsentierten Auswertungen waren Grundlage folgender Publikation: Jantschak et al. (2025): „Das Verfahren der anwendungsbegleitenden Datenerhebung in der frühen Nutzenbewertung“, in „Monitor Versorgungsforschung“ (04/25), S. 34–41. Online verfügbar unter http://doi.org/10.24945/MVF.04.25.1866-0533.2737

Dr. Florian Jantschak
© privat
Literatur
Alle online verfügbaren Quellen wurden am 4. November 2025 abgerufen.
1 Deutscher Bundestag (2019): Entwurf eines Gesetzes für mehr Sicherheit in der Arzneimittelversorgung. Drucksache 19/8753. Online verfügbar unter https://dserver.bundestag.de/btd/19/087/1908753.pdf
2 Gemeinsamer Bundesausschuss (2023): Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Einleitung eines Verfahrens zur Forderung einer anwendungsbegleitenden Datenerhebung und von Auswertungen nach § 35a Absatz 3b des Sozialgesetzbuch Fünftes Buch (SGB V): Talquetamab (rezidiviertes und refraktäres multiples Myelom, mind. 3 Vortherapien). Online verfügbar unter https://www.g-ba.de/downloads/40-268-9888/2023-10-19_AM-RL-XII_Einleitung-AbD_Talquetamab_2023-AbD-005_TrG.pdf
3 Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (2024): AbD-Konzept Marstacimab (Hämophilie A und B). Projekt A24-39. IQWiG-Bericht Nr. 1834. Online verfügbar unter https://www.iqwig.de/download/a24-39_marstacimab_abd-konzept_v1-0.pdf
4 Gemeinsamer Bundesausschuss (2025): Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Einstellung eines Beratungsverfahrens nach § 35a Absatz 3b des Fünften Buches Sozialgesetzbuch (SGB V) Odronextamab (rezidiviertes oder refraktäres follikuläres Lymphom, mindestens 2 Vortherapien); Forderung einer anwendungsbegleitenden Datenerhebung und von Auswertungen. Online verfügbar unter https://www.g-ba.de/downloads/40-268-11267/2025-03-06_AM-RL-XII_Einstellung-Beratungsverfahren_Odronextamab_2023-AbD-009_TrG.pdf
5 European Medicines Agency (2016): Final report on the adaptive pathways pilot. EMA/276376/2016. Online verfügbar unter https://www.ema.europa.eu/en/documents/report/final-report-adaptive-pathways-pilot_en.pdf
6 European Medicines Agency: Conditional marketing authorisation. Online verfügbar unter https://www.ema.europa.eu/en/human-regulatory-overview/marketing-authorisation/conditional-marketing-authorisation
7 Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (2020): Konzepte zur Generierung versorgungsnaher Daten und deren Auswertung zum Zwecke der Nutzenbewertung von Arzneimitteln nach § 35a SGB V - Rapid Report. Version 1.1. Auftrag A19-43. IQWiG-Bericht Nr. 863. Online verfügbar unter https://www.iqwig.de/download/a19-43_versorgungsnahe-daten-zum-zwecke-der-nutzenbewertung_rapid-report_v1-1.pdf
8 Cakir M., Starke P., Nolting A. et al. (2025): Versorgungsnahe Daten zur Bewertung der vergleichenden Effektivität von medizinischen Behandlungen: eine Bestandsaufnahme der verfügbaren Datenquellen in Deutschland unter besonderer Berücksichtigung von Registern. Zeitschrift für Evidenz, Fortbildung und Qualität im Gesundheitswesen; Volume 194, 1-7. Online verfügbar unter https://doi.org/10.1016/j.zefq.2025.01.008
9 Vervölgyi V., Kaiser T. (2024): Datenerhebungen zu Arzneimitteln - eine Perspektive für die Krebsregister. Die Onkologie; Volume 30, 289 - 295. Online verfügbar unter https://doi.org/10.1007/s00761-023-01443-5
10 Gemeinsamer Bundesausschuss (2025). Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Einleitung eines Verfahrens zur Forderung einer anwendungsbegleitenden Datenerhebung und von Auswertungen nach § 35a Absatz 3b des Fünften Buches Sozialgesetzbuch (SGB V): Loncastuximab tesirin (rezidiviertes oder refraktäres diffus großzelliges B-Zell-Lymphom). Online verfügbar unter https://www.g-ba.de/downloads/40-268-11128/2025-01-16_AM-RL-XII_Einleitung-AbD_Loncastuximab-tesirin_2022-AbD-004_TrG.pdf
11 Singer S., Bayer O., Schranz M. et al. (2024): „Patient-reported outcomes“ in medizinischen Registern. Die Onkologie; Volume 30, 304 -311. Online verfügbar unter https://doi.org/10.1007/s00761-024-01494-2
12 Gemeinsamer Bundesausschuss (2024): Workshop anwendungsbegleitende Datenerhebung (AbD) - Zusammenfassung. Online verfügbar unter https://www.g-ba.de/downloads/17-98-5701/Zusammenfassung_AbD_Workshop_final.pdf
13 Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (2022): Wissenschaftliche Ausarbeitung eines Konzeptes zur Generierung versorgungsnaher Daten und deren Auswertung zum Zwecke der Nutzenbewertung nach § 35a SGB V in der Situation des Marktzugangs mehrerer Arzneimittel einer Wirkstoffklasse - Rapid Report. Version 1.0. Auftrag A21-37. IQWiG-Bericht Nr. 1339. Online verfügbar unter https://www.iqwig.de/download/a21-37_abd-bei-marktzugang-mehrerer-arzneimittel-einer-wirkstoffklasse_rapid-report_v1-0.pdf
14 Gemeinsamer Bundesausschuss (2023): Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Einstellung eines Beratungsverfahrens nach § 35a Abs. 3b des Fünften Buches Sozialgesetzbuch (SGB V) Brexucabtagen Autoleucel (rezidivierte oder refraktäre B-Zell Vorläufer akute lymphatische Leukämie); Forderung einer anwendungsbegleitenden Datenerhebung und von Auswertungen. Online verfügbar unter https://www.g-ba.de/downloads/40-268-9652/2023-07-20_AM-RL-XII_Einstellung-Beratungsverfahren_Brexucabtagen-Autoleucel-2022-AbD-008_TrG.pdf
15 Gemeinsamer Bundesausschuss (2025): Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Einstellung eines Beratungsverfahrens nach § 35a Absatz 3b des Fünften Buches Sozialgesetzbuch (SGB V) Epcoritamab (rezidiviertes oder refraktäres follikuläres Lymphom, mindestens 2 Vortherapien); Forderung einer anwendungsbegleitenden Datenerhebung und von Auswertungen. Online verfügbar unter https://www.g-ba.de/downloads/40-268-11272/2025-03-06_AM-RL-XII_Einstellung-Beratungsverfahren_Epcoritamab_2023-AbD-011_TrG.pdf
16 Bickel B., Jantschak F. (2022): Bedeutung der Anwendungsbegleitenden Datenerhebung für die KBV. Springer Medizin, Schriftenreihe „Interdisziplinäre Plattform zur Nutzenbewertung“; Ausgabe 15, 52 - 62. Online verfügbar unter https://www.aerztezeitung.de/Dateien/Weiterentwicklung-des-AMNOG-mit-Augenmass-u-Evidenz-d-570.pdf
17 Sachverständigenrat Gesundheitswesen und Pflege (2025): Preise innovativer Arzneimittel in einem lernenden Gesundheitssystem – Gutachten 2025. Online verfügbar unter https://www.svr-gesundheit.de/fileadmin/Gutachten/Gutachten_2025/SVR_Gutachten_2025.pdf
18 European Medicines Agency (2025): Joint HTAb-regulatory perspectives on understanding evidence challenges, managing uncertainties and exploring potential solutions - Outcome of a workshop series between HTA bodies and regulators. EMA/115125/2025. Online verfügbar unter https://www.ema.europa.eu/en/documents/other/joint-htab-regulatory-perspectives-understanding-evidence-challenges-managing-uncertainties-exploring-potential-solutions_en.pdf
19 Schüßler-Lenz M., Hofner B. (2024): Arzneimittelzulassung im Bereich seltener Erkrankungen: die europäische regulatorische Perspektive am Beispiel der Gen- und Zelltherapeutika. Zeitschrift für Evidenz, Fortbildung und Qualität im Gesundheitswesen; Volume 189, 73 - 81. Online verfügbar unter https://doi.org/10.1016/j.zefq.2024.08.007
20 The European Parliament and the Council of the European Union (2021): Regulation (EU) 2021/2282 of the European Parliament and of the Council of 15 December 2021 on health technology assessment and amending Directive 2011/24/EU. Online verfügbar unter https://eur-lex.europa.eu/legal-content/DE/TXT/PDF/?uri=CELEX:32021R2282
21 HTA Coordination Group (2024): Guidance on the scoping process. Version 1.0. Online verfügbar unter https://health.ec.europa.eu/document/download/7be11d76-9a78-426c-8e32-79d30a115a64_en?filename=hta_jca_scoping-process_en.pdf