ATMP & Orphan Diseases: Datenquellen jenseits von RCT
Perspektiven des BMG auf ATMP und Seltene Erkrankungen
Arzneimitteln für neuartige Therapien spiegeln in besonderem Maße den Fortschritt in der Arzneimittelentwicklung wieder. Sie stehen mit ihren hochinnovativen Versorgungsansätzen für einen Paradigmenwechsel hin zu einer personalisierten Arzneimittelversorgung. Mit dem Modellvorhaben Genomsequenzierung konnte ein Meilenstein für eine innovative Versorgungs- und Forschungsstruktur insbesondere für Patientinnen und Patienten mit Seltenen Erkrankungen erreicht werden.
Veröffentlicht:
Das BMG verfolgt und begleitet die Entwicklungen im ATMP-Bereich gemeinsam mit der für biomedizinische Arzneimittel zuständigen Bundesoberbehörde, dem Paul-Ehrlich-Institut.
© dts-Agentur / picture alliance
Arzneimittel für neuartige Therapien (ATMP)
Bei Arzneimitteln für neuartige Therapien, sogenannte Advanced Therapy Medicinal Products (ATMP), handelt es sich um eine eigenständige Arzneimittelklasse von Humanarzneimitteln, die auf Genen, Zellen oder Geweben basieren. ATMP umfassen Gentherapeutika, somatische Zelltherapeutika sowie biotechnologisch bearbeitete Gewebeprodukte. Kombinierte ATMP, also Kombinationen von ATMP und Medizinprodukten, die bestimmte Voraussetzungen erfüllen, zählen auch zur Gruppe der ATMP.
ATMP spiegeln in besonderem Maße den technologischen und wissenschaftlichen Fortschritt in der Arzneimittelentwicklung wieder. Bei ATMP handelt es sich vielfach um Sprunginnovationen. Aufgrund ihrer besonderen Wirkungsweise bieten sie zum einen Therapieoptionen für Erkrankungen, die bisher mit herkömmlichen Methoden schwer oder nicht zu behandeln sind, mit potenziell heilender Wirkung. Hiervon profitieren bislang besonders Patientinnen und Patienten mit onkologischen Erkrankungen sowie Seltenen Erkrankungen. Zum anderen bringen die innovativen Wirkmechanismen eine neue Komplexität in die Arzneimittelversorgung. Dies gilt insbesondere für die Bereiche Herstellung, Logistik und Anwendung. Sie fordern pharmazeutische Unternehmen, Anwender und zuständige Behörden gleichermaßen.
Seit Inkrafttreten der ATMP-Verordnung Ende 20081 wurden über dreißig ATMP in der Europäischen Union (EU) zugelassen: 4 biotechnologisch bearbeitete Gewebeprodukte, 5 somatische Zelltherapeutika und 21 Gentherapeutika. Aktuell sind insgesamt 21 ATMP zugelassen (siehe Abbildung 1):2
Bei den zugelassenen ATMP handelt es sich ganz überwiegend um Gentherapeutika (17 Zulassungen, Stand 12/2025).
Beispielhaft für diese hochinnovative Arzneimittelgeneration stehen die CAR-T-Zelltherapien: Dabei werden patienteneigene Immunzellen (T-Zellen) außerhalb des Körpers (ex vivo) mit einem genetisch veränderten (chimären) Antigenrezeptor (CAR) versehen. Dies erfolgt mit Hilfe von sogenannten Genfähren (viralen Vektoren), welche die genetische Information für den CAR in das Genom der T-Zellen übertragen. Die so veränderten T-Zellen können Krebszellen spezifisch erkennen und bekämpfen. Nach der ersten Zulassung eines CAR-T-Zelltherapeutikums im Jahr 2018 sind in der EU aktuell bereits sieben CAR-T-Zelltherapeutika zugelassen (hämatologische und lymphatische Krebserkrankungen). Die Behandlung diverser solider Tumore wird international in verschiedenen Studien erprobt. Des Weiteren wurden erste Erfolge in der Therapie von Autoimmunerkrankungen erzielt. Klinische Prüfungen zu CAR-T-Zellen in Kombinationstherapie, als Zweitlinientherapie oder auch gegen Hämophilie laufen derzeit.
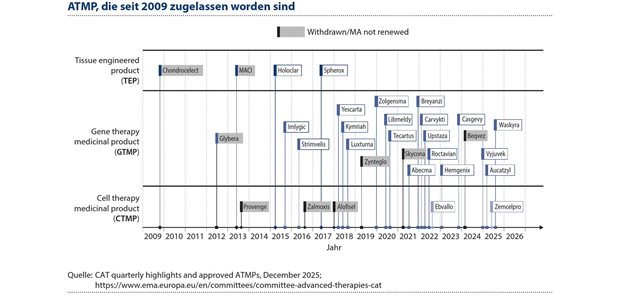
Abbildung 1: Seit Inkrafttreten der ATMP-Verordnung Ende 2008 sind über 30 ATMP in der Europäischen Union zugelassen worden, darunter sind 21 Gentherapeutika.
© Springer Medizin Verlag
Das BMG verfolgt und begleitet die Entwicklungen im ATMP-Bereich gemeinsam mit der für biomedizinische Arzneimittel zuständigen Bundesoberbehörde, dem Paul-Ehrlich-Institut. Dies gilt für das Bundesministerium insbesondere im Hinblick auf die regulatorischen, ökonomischen wie auch infrastrukturellen Herausforderungen, die diese hochinnovativen Arzneimittel für das Gesundheitssystem mit sich bringen.
ATMP tragen maßgeblich zur Dynamik in der Arzneimittelentwicklung bei. Sie haben das Potenzial, die bestehenden Märkte und Geschäftsmodelle grundlegend zu verändern (hoher Innovationsdruck) und neue Wertschöpfungsketten zu etablieren. Immer mehr Unternehmen, von Biotech-Start-Ups bis hin zu großen, multinationalen Pharmaunternehmen, investieren in ATMP als Wachstumsfeld. Neue Geschäftsmodelle entstehen, ebenso wie neue Kooperationen und Netzwerke.
Die Zahl der ATMP in klinischer Entwicklung nimmt seit Jahren stetig zu. Weitere innovative Arzneimittelzulassungen, insbesondere im Bereich der Gentherapien, sind zu erwarten. Damit können einer steigenden Anzahl von Patientinnen und Patienten hochinnovative und personalisierte Therapieoptionen angeboten werden. Diese liegen eher im hochpreisigen Segment. Wir bewegen uns damit in einem strukturellen Spannungsfeld zwischen der zeitnahen Verfügbarkeit von innovativen Arzneimitteltherapien unter Wahrung einer sicheren und qualitätsgeprüften Versorgung der Patientinnen und Patienten und der Gewährleistung der Finanzierbarkeit im solidarischen System der Gesetzlichen Krankenversicherung.
Nicht zuletzt werden auch Fortschritte in weiteren Technologiefeldern wie z. B. der Künstlichen Intelligenz (KI) sowie die fortschreitende Digitalisierung, die Entwicklung neuer und effizienter Produktionstechnologien, z. B. Plattformtechnologien, als auch die fortschreitende Automatisierung, die Forschung und Entwicklung von hochinnovativen Arzneimittel immens beschleunigen und neue Wege ebnen.
Evidenzgenerierung: Schaffung und Ausbau von Dateninfrastrukturen
Mit dem Start der Nationalen Strategie Genommedizin – genomDE im Februar 2019 verfolgt das BMG das Ziel, die Vorteile der Genommedizin Patientinnen und Patienten langfristig zugänglich zu machen. Die Genommedizin ermöglicht es inzwischen, Krankheiten immer besser zu diagnostizieren und zu behandeln sowie individuell angepasste Präventionsmaßnahmen einzuleiten. Diese personalisierte, auf das individuelle Erbgut eines Menschen angepasste Medizin bietet damit erhebliche Vorteile. Davon können Patientinnen und Patienten mit Seltenen Erkrankungen im besonderen Maße profitieren.
Wesentlicher Bestandteil der Nationalen Strategie genomDE ist das Modellvorhaben Genomsequenzierung nach Paragraf 64e des Fünften Buches Sozialgesetzbuch (SGB V). Es umfasst eine qualitätsgesicherte standardisierte und nach dem Stand von Wissenschaft und Technik zu erbringende Diagnostik und Therapiefindung mittels Genomsequenzierung bei Seltenen und onkologischen Erkrankungen. Im Juli 2024 konnte das Modellvorhaben erfolgreich starten. Wichtige Grundlagen hierfür sind:
ein bundeseinheitlicher Vertrag zwischen GKV-Spitzenverband und Leistungserbringern, der im Juli 2024 geschlossen wurde und dem im September 2024 auch die PKV beigetreten ist, d.h. eine einheitliche Kostenübernahme von Diagnostik und Therapiefindung auf Basis von gestuften Kostenpauschalen;
eine bundesweite, dezentral organisierte Dateninfrastruktur mit BfArM als Plattformträger und RKI als zentraler Vertrauensstelle zum Schutz der sensiblen genomischen und klinischen Daten der Patientinnen und Patienten;
standardisiert erhobene, hochqualitative genomische und klinische Daten (auf Grundlage der Genomdatenverordnung) zur Nutzung für Versorgungs- und (einwilligungsbasiert) Forschungszwecke, z. B. im Rahmen der Prüfung neuer Arzneimitteltherapien.
Das Vorhaben konnte nur durch ein intensives und konsequentes Zusammenwirken aller am Modellvorhaben Beteiligten starten4 und wird von diesem gemeinsamen Bewusstsein weiterhin profitieren. Mit einer mindestens fünfjährigen Laufzeit soll das Modellvorhaben die Integration der Genommedizin in die Gesundheitsversorgung in Deutschland ermöglichen und den Weg in die Regelversorgung ebnen. Dafür wird es kontinuierlich von unabhängiger Stelle evaluiert.
Mit dem Modellvorhaben investiert die Gesetzliche Krankenversicherung (GVK) während der Laufzeit bis zu 700 Mio. Euro und bereitet damit den Weg für eine bessere, innovative Versorgung für die Versicherten. Dies geschieht weltweit erstmalig – Deutschland nimmt damit eine Vorreiterrolle ein5. An dem Modellvorhaben beteiligen sich aktuell 30 Universitätskliniken (Stand 12/2025), die auf der Grundlage eines einheitlichen Datenkranzes6 gezielt sowohl klinische als auch genomische Daten über die behandelten Patientinnen und Patienten erheben. In einem Zulassungsverfahren wurde vom GKV-Spitzenverband (GKV-SV) vorab geprüft, welche Krankenhäuser über die notwendigen personellen und technischen Voraussetzungen für diese komplexen Leistungen in einem qualitätsgesicherten Prozess verfügen.
Durch die Zusammenführung von klinischen und genomischen Daten in einer sicheren Dateninfrastruktur wird – im Sinne einer wissensgenerierenden Versorgung – ein Erkenntnisgewinn ermöglicht, der sowohl den teilnehmenden Patientinnen und Patienten als auch zukünftig weiteren betroffenen Personen zugutekommen kann. Die von den Patientinnen und Patienten erhobenen Daten können neben der direkten Versorgung mit einer entsprechenden Einwilligung auf Antrag auch für die Forschung genutzt werden. Dazu werden die Daten pseudonymisiert in einer sicheren Verarbeitungsumgebung bereitgestellt.
So können mögliche ursächliche Veränderungen im Erbgut und molekulare Mechanismen erforscht, eine gezieltere und schnellere Entwicklung von Medikamenten ermöglicht sowie differenziert Erkrankungsrisiken, Therapiemöglichkeiten und -verläufe diagnostiziert und prognostiziert werden. Damit kann das Modellvorhaben auch einen wichtigen Vorteil für den Pharmastandort Deutschland erbringen.
Das Modellvorhaben Genomsequenzierung ist aus unserer Sicht ein Meilenstein für die Versorgung von Patientinnen und Patienten wie auch für die Weiterentwicklung der personalisierten Medizin in Deutschland. Damit steht das modernste und anspruchsvollste Verfahren zur Verfügung, um das Vorliegen einer Seltenen Erkrankung mit einer genetischen Ursache zu untersuchen und Therapieempfehlungen treffen zu können. Davon profitieren z. B. im pädiatrischen Bereich junge Patientinnen und Patienten wie auch deren Angehörige.
Aktuell wird von Seiten des Bundesministeriums für Gesundheit und des Plattformträgers bereits an der zukünftigen Datenverknüpfung gearbeitet. Im Vordergrund steht dabei die Verknüpfung mit den Daten des Forschungsdatenzentrums Gesundheit. Ein weiteres großes Vorhaben ist der europäische Anschluss des Modellvorhabens im Sinne der europäischen 1+Million Genomes-Initiative7 und im Einklang mit den Regelungen zum Europäischen Gesundheitsdatenraum.
Das Modellvorhaben Genomsequenzierung schafft eine innovative Forschungs- und Versorgungsstruktur, die als Vorbild für weitere innovative Bereiche dienen kann – im Sinne einer lernenden, evidenzbasierten und nachhaltig finanzierbaren Gesundheitsversorgung.8 Aufbauend auf den positiven Erfahrungen mit dem Modellvorhaben Genomsequenzierung und einem ersten Erfahrungsaustausch mit Expertinnen und Experten konzipiert das BMG derzeit ein Modellvorhaben für ATMP-Innovationszentren. Ziel ist es, Patientinnen und Patienten, für die es bisher keine zugelassenen Therapien gibt, eine Therapieoption mit ATMP wie z. B. CAR-T-Zelltherapien in einem strukturierten, wissensgenerierenden, qualitätsgesicherten Versorgungsablauf im Rahmen eines Modellvorhabens anzubieten.
Biotechnologische Plattformen wie CAR-T oder auch Genscheren bieten große Chancen für Patientinnen und Patienten, stellen aber auch höchste Anforderungen an die technologische Kompetenz der Kliniken und die Qualitätssicherung der Herstellungsverfahren. Das Modellvorhaben ATMP-Innovationszentren soll sicherstellen, dass spezialisierte Zentren in Deutschland mit der Entwicklung Schritt halten und geeignete Strukturen aufgebaut werden.
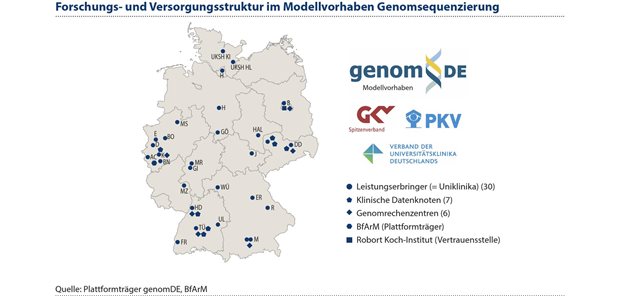
Abbildung 2: Das Modellvorhaben Genomsequenzierung schafft eine innovative Forschungs- und Versorgungsstruktur, die als Vorbild für weitere Bereiche dienen kann – im Sinne einer lernenden, evidenzbasierten Gesundheitsversorgung.
© Springer Medizin Verlag
Bei der weiteren Konzeption des Modellvorhabens ATMP-Innovationszentren wird auch der nach Paragraf 4c des Arzneimittelgesetzes bestehende Auftrag für die Erstellung eines Konzepts für ein indikationsbezogenes ATMP-Register mitberücksichtigt. Das Konzept ist bis zum 31. Dezember 2027 vorzulegen; erste Arbeiten dazu haben begonnen.
Ausgewählte EU-Initiativen im Bereich Biotechnologie
Mit der am 2. Juli 2025 veröffentlichten EU-Strategie für die Biowissenschaften (Life Science Strategy)9 verfolgt die Europäische Kommission das Ziel, die Europäische Union bis zum Jahr 2030 weltweit wieder an die Spitze der Innovation in den Lebenswissenschaften zu bringen. Die EU-Strategie, die mit mehr als 10 Milliarden Euro jährlich aus dem laufenden EU-Haushalt unterstützt wird, sieht einen koordinierten Ansatz für die gesamte Wertschöpfungskette der Lebenswissenschaften vor. Als gesundheitspolitische Maßnahmen sind z. B. Erleichterungen für länderübergreifende klinische Studien und eine Stärkung der europäischen Infrastrukturen für klinische Forschung vorgesehen. Dies umfasst auch die Schaffung von Europäischen ATMP-Exzellenzzentren. Der Marktzugang für biowissenschaftliche Innovationen soll beschleunigt werden.10 Ein besonderer Fokus liegt auch auf der Datennutzung und dem Einsatz von KI für bahnbrechende Innovationen.
Des Weiteren hat die Europäische Kommission am 16. Dezember 2025 ihren Entwurf für einen Europäischen Rechtsakt zur Biotechnologie für den Gesundheitsbereich vorgelegt (sog. EU Biotech Act I).11 Der Rechtsakt hat für die Kommission eine hohe Priorität und ist Teil politischer Leitlinien und mehrerer Kommissions-Initiativen bzw. -Strategien (Förderung der Biotechnologie, Life Science Strategy). Mit dem Vorschlag will die Kommission die Gesundheitsbiotechnologie-Branche in der EU stärken. Wesentliche Schwerpunkte sind die Projektförderung und die Verbesserung des Patentschutzes durch Verlängerung des ergänzenden Schutzzertifikats, Beschleunigungen und Vereinfachungen im Bereich der klinischen Prüfung (auch im Hinblick auf ATMP), darüber hinaus die Unterstützung von Gesundheitsinnovationen sowie Maßnahmen im Bereich der Datennutzung und KI.
Mit Blick auf die wachsende Bedeutung der Biotechnologie für die Arzneimittelversorgung und die steigende wirtschaftspolitische sowie strategische Bedeutung begrüßen wir die Initiative der Europäischen Kommission. Es ist wichtig, zügig voranzukommen, damit Patientinnen und Patienten auf der einen Seiten schnellen Zugang zu wissenschaftlichen Fortschritten und Innovationen haben und davon profitieren können, und damit auf der anderen Seite die globale Wettbewerbsfähigkeit der EU gestärkt wird.
Perspektiven zu Kosten, Erstattung, HTA
Arzneimittelausgaben
Für das 1. bis 3. Quartal 2025 weisen die amtlichen Statistiken einen Anstieg der Arzneimittelausgaben um sechs Prozent (+ 2,5 Milliarden Euro) aus. Damit liegt die Steigerungsrate unterhalb des Anstiegs der GKV-Gesamtausgaben im selben Zeitraum, die bei rund 7,8 Prozent lag, jedoch weiterhin höher als im Durchschnitt der Jahre 2013 bis 2024 (5,6 Prozent) und deutlich über der langfristigen Entwicklung der Einnahmen.
Die Dynamik im Arzneimittelbereich liegt 2025 unterhalb der zwei weiteren großen Ausgabenblöcke Krankenhausbehandlungen mit einem Anstieg von 9,9 Prozent (+ 7,4 Milliarden) und ambulant-ärztliche Behandlung mit einem Anstieg von 7,6 Prozent (+ 2,9 Milliarden). Die Beitragseinnahmen sind im gleichen Zeitraum um 5,3 Prozent angestiegen. In 2024 waren die Arzneimittelausgaben, insbesondere auch aufgrund der Ende 2023 ausgelaufenen (einmaligen) Anhebung des Herstellerabschlags, um 10,7 Prozent (+ 5,4 Milliarden Euro) angestiegen.
Der Ausgabenanstieg bei Arzneimitteln ist einerseits durch die Kosten- und Preisdynamik bei hochinnovativen Patentarzneimitteln geprägt. Patentgeschützte Arzneimittel machen über 50 Prozent der Arzneimittelausgaben aus, bei unter 10 Prozent der Verordnungen. Das zeigt, dass die ärztlichen Verordnungen teurer innovativer Wirkstoffe stark auf spezifische Patientengruppen fokussiert sind, z. B. in der Onkologie. Für die Jahre 2026-2027 ist für Arzneimittel weiterhin auch wegen neuer Entwicklungen, z. B. der personalisierten Therapie, eine dynamische Entwicklung prognostiziert. Nach neuen Zahlen des Wissenschaftlichen Instituts der AOK12 lag die Veränderungsrate der Nettokosten für diese Arzneimittel bei 6,9 Prozent, d.h. auch das Marktsegment der Nicht-Patentarzneimittel hat im Jahr 2024 an Dynamik dazugewonnen.
Der Koalitionsvertrag sieht vor, zur Vermeidung weiterer Anhebungen der Beitragssätze die Finanzsituation der GKV zu stabilisieren durch ein Gesamtpaket aus strukturellen Anpassungen und kurzfristigen Maßnahmen, wobei zugleich eine hohe Qualität und ein hohes Niveau der Leistungen gesichert sein sollen. Vorschläge soll eine Expertenkommission unter Beteiligung der Sozialpartner erarbeiten.
Der Koalitionsvertrag sieht gleichzeitig vor, Deutschland zum weltweit innovativsten Chemie-, Pharma- und Biotechnologiestandort zu machen. Die Rahmenbedingungen für die Entwicklung und Produktion von Arzneimitteln, Wirkstoffen und Medizinprodukten sollen weiter verbessert werden. Die industrielle Gesundheitswirtschaft, insbesondere die pharmazeutische Industrie und Medizintechnik, soll als Leitwirtschaft gestärkt werden. Es ist vorgesehen, das AMNOG mit Blick auf die „Leitplanken“ und auf personalisierte Medizin weiterzuentwickeln.
Preisbildung & Pay for Performance
Gen- und Zelltherapien mit einmaliger Anwendung und teilweise sehr hohen Einmalkosten sind bereits seit einigen Jahren in der deutschen Versorgung. Sie stehen den betroffenen Patientinnen und Patienten unmittelbar nach Markteinführung zur Verfügung und haben das AMNOG-Verfahren erfolgreich durchlaufen.
Aktuell ist die Ausgabenbelastung der GKV durch diese Therapieformen – trotz der sehr hohen Einmalpreise – auf Grund der sehr kleinen Patientengruppen und einer beobachtbaren geringen Marktdurchdringung noch untergeordnet. Perspektivisch könnte aber auch die Versorgung von Patientinnen und Patienten mit häufigen Erkrankungen durch Gen- und Zelltherapien erreicht werden, beispielsweise neurologische Erkrankungen wie die Parkinson-Erkrankung.
Diese Arzneimitteltherapien verdeutlichen somit das Spannungsfeld zwischen dem berechtigten Interesse an einer möglichst zeitnahen Verfügbarkeit von neuen Therapien und der Gewährleistung der finanziellen Stabilität der GKV. Die Gen- und Zelltherapien müssen daher nicht nur für neue medizinische Indikationen weiterentwickelt werden, sondern die Weiterentwicklung muss auch die Effizienz der Produktionsprozesse adressieren. Die Prozesse müssen schneller, einfacher und stärker automatisiert werden, um Gentherapien auch für breite Patientengruppen verfügbar zu machen.
Sehr hohe Preise bei Gentherapien stellen die solidarische Finanzierung der gesetzlichen Krankenversicherung auf die Probe. Hierbei wird auch die Option des Pay-for-Performance-Ansatzes („P4P“) zwischen den Beteiligten diskutiert. Bei Pay-for-Performance-Verträgen handelt es sich um erfolgsabhängige Vergütungsmodelle, bei denen die Kosten einer Arzneimitteltherapie an den jeweiligen Behandlungserfolg gekoppelt werden. Aufgrund der hohen Einmalkosten und der bestehenden Unsicherheit der Langzeiteffekte werden diese im Zusammenhang mit Gentherapien vermehrt in Betracht gezogen. Die bereits bekannt gewordenen Einigungen zwischen dem GKV-SV und einzelnen Unternehmen zu P4P-Erstattungsbeträgen (z. B. Zynteglo®, Roctavian® oder Hemgenix®) bestätigen dies.
Allerdings sind Pay-for-Performance-Verträge abhängig von der Ausgestaltung mit hohen Transaktionskosten verbunden. Dies gilt insbesondere, weil individuelle Verläufe über längere Zeiträume beobachtet, gemessen und ausgewertet werden, um die zugrundliegenden Erfolgsparameter im Einzelfall zu messen. Es ist die Entscheidung der jeweiligen Vertragsparteien, ob und in welcher Ausgestaltung erfolgsabhängige Vergütungsmodelle im konkreten Einzelfall auf kollektivvertraglich- und/oder selektivvertraglicher Basis vereinbart werden. Der Themenkomplex wird auch im Pharmadialog eine Rolle spielen.
EU-HTA
Auf EU-Ebene werden derzeit die ersten gemeinsamen klinischen Bewertungen neuer Arzneimittel durchgeführt. Entsprechend der schrittweisen Ausweitung der Verordnung (EU) 2021/2282 (EU-HTA-Verordnung), wird zunächst mit Onkologika und ATMP begonnen. Aktuell befinden sich auf EU-Ebene zwölf Produkte in der Bewertung. Mit ersten Abschlüssen der Bewertungen ist ungefähr im zweiten Quartal 2026 zu rechnen.
Die gemeinsam bewerteten Arzneimittel unterliegen bei Markteinführung in Deutschland weiterhin der Nutzenbewertung nach Paragraf 35a SGB V. Dabei sind die Vorgaben der EU-HTA-Verordnung für die nationalen HTA-Verfahren zu beachten, zu deren Durchführung die Arzneimittel-Nutzenbewertungsverordnung mit Wirkung vom 8. März 2025 angepasst wurde.13 Mit den zunächst lediglich geringfügigen Änderungen sollen europäisches und nationales Verfahren sachgerecht verzahnt werden. Insbesondere entscheidet der pharmazeutische Unternehmer, inwieweit er die auf EU-Ebene eingereichten Nachweise, die er aufgrund des europäischen Doppelanforderungsverbots nicht erneut übermitteln muss, für die nationale Nutzenbewertung verwenden möchte, und nimmt auf die entsprechenden Nachweise Bezug (Verweislösung).
Das BMG begleitet die Einführungsphase der gemeinsamen klinischen Bewertungen auf EU-Ebene intensiv, wird die Ergebnisse auswerten und gegebenenfalls weitere notwendige Änderungen am nationalen Nutzenbewertungsverfahren vornehmen, insbesondere mit dem Ziel, Doppelarbeit zu vermeiden.
Ausblick
Das aktuelle globale Umfeld mit seinen Entwicklungen bedeutet neue Herausforderungen auch für die pharmazeutische Industrie. Insbesondere die US-Pharmapolitik mit Zollvereinbarungen und dem Most-Favoured-Nation-Konzept sind Herausforderungen für die pharmazeutische Industrie.
Trotz der politischen Grundsatzeinigung der EU mit den USA im Juli 2025 zu Zöllen auch für Arzneimittel, sind weitere Diskussionen hierzu nicht ausgeschlossen. Zudem schließt die US-Regierung unter Anwendung des sogenannten Most-Favoured-Nation-Konzeptes Vereinbarungen mit Pharmaunternehmen mit dem Ziel, zu Preissenkungen in den USA auf dem Niveau vergleichbar entwickelter Staaten zu kommen und gleichzeitig zu Preiserhöhungen in diesen Staaten.
Umso wichtiger ist es daher, die pharmazeutische Industrie als Leitwirtschaft in Deutschland weiter zu stärken, wie es der Koalitionsvertrag vorsieht. Die pharmazeutische Industrie ist eine tragende Säule des Wirtschaftsstandorts Deutschland. Neben den Vorteilen für Wachstum und Beschäftigung, kommt die Innovationskraft der Pharmaindustrie unmittelbar auch der Versorgung von Patientinnen und Patienten zugute.
Deshalb führt die Bundesregierung unter Federführung des BMG den Pharma- und Medizintechnikdialog durch. Ziel des Dialoges und der daraus zu entwickelnden Strategie der Bundesregierung ist es, klare Impulse für Forschung, Entwicklung sowie Produktion setzen und die Wettbewerbsfähigkeit der Branche zu stärken und damit Deutschland als globalen Innovations- und Produktionsstandort zu positionieren. Es sollen aktuelle Herausforderungen und zukünftige Entwicklungen identifiziert werden, um gemeinsam tragfähige Lösungen zu erarbeiten. In den Dialogprozess sind alle fachlich betroffenen Ministerien eingebunden, damit koordinierte Rahmenbedingungen in allen Bereichen geschaffen werden, die Innovationen und Investitionen fördern.

Thomas Müller
© privat
Thomas Müller ist approbierter Arzt und Apotheker. Er studierte in Berlin und London Pharmazie und Humanmedizin. Nach Stationen in der Dermatologischen Abteilung der Berliner Charité und in Krankenhausapotheken der Universitätskliniken von Erlangen und Rostock übernahm er die Leitung der Krankenhausapotheke am Universitätsklinikum Rostock.
Von 2007 bis 2018 war Thomas Müller Leiter der Abteilung Arzneimittel des Gemeinsamen Bundesausschusses (G-BA) in Berlin. Im Rahmen seiner Tätigkeit im G-BA spielte Thomas Müller eine Schlüsselrolle bei der erfolgreichen Gestaltung, Planung und Umsetzung der frühen Nutzenbewertung und Preisbildung bei Arzneimitteln mit neuen Wirkstoffen (AMNOG) in Deutschland.
Seit 2018 leitet er die Abteilung 1 für Arzneimittel, Medizinprodukte, Biotechnologie im Bundesministerium für Gesundheit. Er ist Lehrbeauftragter der Universität Bonn.

Dr. Jana Straßburger
© BMG
Dr. Jana Straßburger ist promovierte Juristin. Seit Herbst 2023 leitet Dr. Jana Straßburger das Referat „Biotechnologische Innovation, Nanotechnologie und Gentechnik“ im Bundesministerium für Gesundheit (BMG). Von 2007 bis 2023 war sie in verschiedenen Bereichen der Abteilung „Arzneimittel, Medizinprodukte, Biotechnologie“ im BMG tätig. Zuvor war sie Wissenschaftliche Mitarbeiterin der Juristischen Fakultät der Technischen Universität Dresden und Mitglied der Ethikkommission des Universitätsklinikums Carl Gustav Carus an der TU Dresden.
Literatur
*Mit bestem Dank für die Unterstützung durch das Referat „Versorgung mit neuen Arzneimitteln und Pandemiearzneimitteln“, BMG, zu Arzneimittelkosten, Erstattung und HTA.
1 Verordnung (EG) Nr. 1394/2007 des Europäischen Parlaments und des Rates vom 13. November 2007 über Arzneimittel für neuartige Therapien und zur Änderung der Richtlinie 2001/83/EG und der Verordnung (EG) Nr. 726/2004, ABl. EU vom 10.12.2007, L 324/121.
2 Für Waskyra® (Etuvetidigene Autotemcel), eine Gentherapie für das Wiskott-Aldrich-Syndrom (WAS), hat der CHMP im November 2025 eine positive Empfehlung abgegeben; die Zulassung durch die Europäischen Kommission steht noch aus. Mit Waskyra® steigt die Zahl der zugelassenen ATMP auf 22.
3 vfa, CRISPR-basierte Gentherapien, siehe unter: https://www.vfa.de/de/forschung-entwicklung/pharmaforschung/crispr-basierte-gentherapien, 13. Februar 2024.
4 Weitere Einzelheiten siehe bei Till et al., Germany’s national genomDE strategy, Nature Medicine vom 15.10.2025, unter https://www.nature.com/articles/s41591-025-03991-2.
5 Gemeinsame Pressemitteilung des GKV-Spitzenverbands und VUD vom 1. Juli 2024: https://www.gkv-spitzenverband.de/gkv_spitzenverband/presse/pressemitteilungen_und_statements/pressemitteilung_1848228.jsp und https://www.uniklinika.de/aktuellespresse/presse/presse-detail/gemeinsame-pressemitteilung-des-vud-und-des-gkv-sv-grundstein-fuer-das-modellvorhaben-genomsequenzierung-gelegt-erstmals-wird-die-diagnostik-in-der-versorgung-und-fuer-zukuenftige-anwendungsfaelle-erprobt/.
6 Zum einheitlichen Datenkranz siehe Anlage zur Verordnung zum Modellvorhaben zur umfassenden Diagnostik und Therapiefindung mittels Genomsequenzierung bei seltenen und bei onkologischen Erkrankungen (Genomdatenverordnung - GenDV) vom 8. Juli 2024, unter https://www.gesetze-im-internet.de/gendv/.
7 https://digital-strategy.ec.europa.eu/de/policies/1-million-genomes.
8 Nach Einschätzung des GKV-Spitzenverbandes und des Verbandes der Universitätsklinika kann die Kombination aus breitem Zugang, einheitlichen und hohen Qualitätsstandards der Universitätsmedizin und einer datengestützten Evaluation ein Vorbild sein für künftige Innovationen wie etwa im Bereich der Gen- und Zelltherapien, siehe Bussmann und Wolff, Ein Impulsgeber für die Zukunft der Genommedizin, Beitrag vom 15.9.2025, https://observer-gesundheit.de/ein-impulsgeber-fuer-die-zukunft-der-genommedizin/; Pressemitteilung von GKV-SV und VUD vom 26.2.2025 zum Thema Seltene Erkrankungen unter https://www.uniklinika.de/fileadmin/user_upload/Pressemitteilungen/2025/VUD_GKV-PM_Seltene_Erkrankungen_250226.pdf
9 https://research-and-innovation.ec.europa.eu/strategy/strategy-research-and-innovation/jobs-and-economy/strategy-european-life-sciences_en.
10 Für innovative Arzneimittel, die dem zentralen Zulassungsverfahren unterfallen, enthält bereits das EU Pharmapaket einen Maßnahmenkatalog zur Verbesserung bzw. Beschleunigung des Marktzugangs.
11 https://ec.europa.eu/info/law/better-regulation/have-your-say/initiatives/14627-Biotech-Act_en.
12 Schröder, H, Thürmann, P et al; Arzneimittelkompass 2025, S. 294; Springer Verlag.
13 Erste Verordnung zur Änderung der Arzneimittel-Nutzenbewertungsverordnung vom 4. März 2025, BGBl. 2025 I Nr. 75 vom 7. März 2025. Referentenentwurf und Verordnungsbegründung sind unter https://www.bundesgesundheitsministerium.de/service/gesetze-und-verordnungen/detail/arzneimittel-nutzenbewertungsverordnung.html abrufbar. Der Gemeinsame Bundesausschuss hat seine Verfahrensordnung mit Beschluss vom 17. Juli 2025 (BAnz AT 17.11.2025 B4) entsprechend angepasst.