Perampanel
Eisai kritisiert IQWiG-Votum
Perampanel durchläuft zum zweiten Mal den Prozess der Nutzenbewertung. Das IQWiG hat den Zusatznutzen erneut nicht anerkannt.
Veröffentlicht:FRANKFURT/MAIN. Eisai zeigt sich enttäuscht über die Bewertung des IQWiG, laut der für Fycompa® (Perampanel) im Vergleich zu vom GBA bestimmten herkömmlichen Antiepileptika kein Zusatznutzen belegt sei.
Perampanel ist ein Antiepileptikum, das selektiv an AMPA-Rezeptoren angreift. Die Arznei wurde als Zusatztherapie bei fokalen epileptischen Anfällen mit oder ohne sekundäre Generalisierung bei Patienten ab 12 Jahren zugelassen.
"Das IQWiG hat den Zusatznutzen von Fycompa® erneut nicht anerkannt, und zwar ausschließlich aufgrund methodologischer, nicht jedoch klinischer Erwägungen. Unsere vorrangige Sorge gilt den Patienten, und wir sind der Meinung, dass in diesem Bericht mehr als 4000 Menschen mit Epilepsie in Deutschland ignoriert werden, denen Fycompa® bereits geholfen hat. Wir bleiben zuversichtlich, dass der G-BA eine umfassendere Sichtweise wählt, die anerkennt, dass weitere Behandlungsoptionen in der Zusatztherapie für Patienten mit Epilepsie immer benötigt werden", wird Gary Hendler zitiert, der Präsident und CEO von Eisai EMEA.
"Im Bericht des IQWiG wurden die deutschen Epilepsiepatienten nicht berücksichtigt, die bereits vom Zusatznutzen von Perampanel profitieren. Es liegen ernstzunehmende Erfahrungswerte vor, und ich selbst habe den individuellen Zusatznutzen, den dieses Therapeutikum bei Patienten mit refraktären fokalen Epilepsien haben kann, in einer Publikation beschrieben", so Professor Bernhard Steinhoff vom Epilepsiezentrum Kork in Kehl-Kork in der Mitteilung des Unternehmens.
Bei der frühen Nutzenbewertung durchgefallen
Das IQWiG komme in seiner Bewertung zu dem Schluss, dass Eisai von der vom GBA festgelegten zweckmäßigen Vergleichstherapie abweiche, so der Hersteller.
Die Bewertung beinhalte keine Aussage in Bezug auf die nachgewiesene klinische Wirksamkeit und Sicherheit von Perampanel, die in den beim GBA und zur Erreichung der EU-weiten Zulassung im September 2012 eingereichten Studien gezeigt wurde.
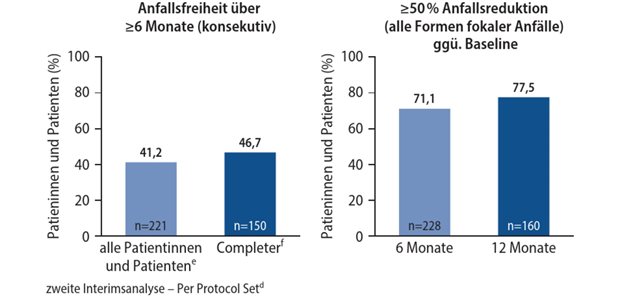
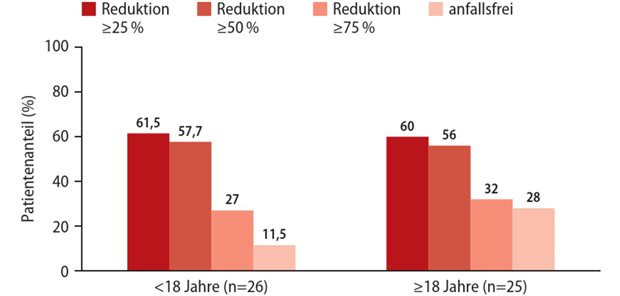
Die Wirksamkeit und Verträglichkeit von Perampanel in der klinischen Praxis als Zusatztherapie fokaler Anfälle wurden in einer sechsmonatigen multizentrischen Beobachtungsstudie an neun Epilepsiezentren in Deutschland und Österreich untersucht, erinnert das Unternehmen Eisai.
Die Hälfte der 281 Patienten mit stark refraktärer Epilepsie, die an der Studie teilnahmen, erreichte eine Verringerung der Anfallshäufigkeit um mindestens 50 Prozent, und 15 Prozent wurden unter Perampanel als Zusatztherapie anfallsfrei.
Bei der frühen Nutzenbewertung im vergangenen Jahr war dem Antiepileptikum vom GBA kein Zusatznutzen zugesprochen worden. Eisai hatte daraufhin Perampanel in Deutschland aus dem Vertrieb genommen wird. Für die mit Perampanel behandelten Patienten wurde ein Programm eingerichtet, das weiterhin den Zugang zur Arznei ermöglicht.
Im Frühjahr 2014 hatte der Hersteller dann das Antiepileptikum zur erneuten Nutzenbewertung eingereicht. (eb)