EU-Zulassung
Abrocitinib: neue Option bei atopischer Dermatitis
Berlin. Die Europäische Kommission hat Cibinqo® (Abrocitinib) für die Behandlung von Erwachsenen mit mittelschwerer bis schwerer atopischer Dermatitis, die für eine systemische Therapie infrage kommen, zugelassen.
Die Zulassung des einmal täglich oral anzuwendenden Januskinase 1 (JAK1)-Inhibitors erfolgte für die Dosierungen 100 mg und 200 mg. Darüber hinaus wurde eine Dosis von 50 mg zur Behandlung bei mittelschwerer bis schwerer atopischer Dermatitis speziell bei Patienten mit mittelschwerer und schwerer Niereninsuffizienz oder bei bestimmten Patienten, die mit Cytochrom-P450 2C19 inhibierenden Wirkstoffen behandelt werden, zugelassen. Es wird angenommen, dass die Hemmung von JAK1 mehrere Zytokine moduliert, die an der Pathophysiologie der atopischen Dermatitis beteiligt sind, darunter die Interleukine IL-4, IL-13, IL-31, IL-22 und das thymische stromale Lymphopoietin (TSLP).
Entwicklungsprogramm JADE liefert Daten für die Zulassung
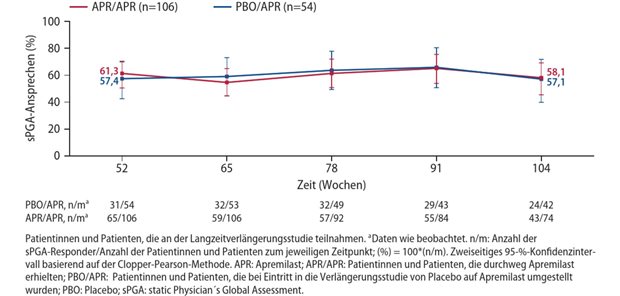
Die Zulassung stützt sich auf die Ergebnisse von fünf klinischen Studien des globalen Entwicklungsprogramms JADE (JAK1 Atopic Dermatitis Efficacy and Safety), darunter vier Phase III-Studien sowie eine noch laufende, offene Langzeitverlängerungsstudie. In den Studien wurde die Verbesserung der atopischen Dermatitis untersucht, die anhand des Investigator Global Assessment (IGA), des Eczema Area and Severity Index (EASI) und der Peak Pruritus Numerical Rating Scale (PP-NRS) gemessen wurden. Abrocitinib zeigte deutliche Verbesserungen hinsichtlich der Linderung von Symptomen und der Krankheitskontrolle im Vergleich zu Placebo.
In einer Studie, die einen aktiven Kontrollarm mit Dupilumab umfasste und in der Patienten mit topischer Hintergrundtherapie berücksichtigt wurden, hatte Abrocitinib 200 mg nach zwei Wochen eine stärkere Linderung des Juckreiz gebracht als Dupilumab. Der JAK1-Inhibitor zeigte auch ein konsistentes Sicherheitsprofil über alle Studien hinweg, einschließlich einer Langzeitverlängerungsstudie, und hatte ein günstiges Nutzen-Risiko-Profil.
Die häufigsten unerwünschten Ereignisse, die bei ≥ 5% der PatientInnen unter Abrocitinib auftraten, waren Übelkeit (15,1%) und Kopfschmerzen (7,9%). Die häufigsten schwerwiegenden unerwünschten Ereignisse waren Infektionen (0,3%). (eb)
Quelle: Mitteilung der Pfizer Pharma GmbH