Proteinbasierter COVID-19-Impfstoff
EMA empfiehlt Zulassung von Novavax’ Corona-Vakzine Nuvaxovid
Der fünfte SARS-CoV-2-Impfstoff kann in der EU bald eingesetzt werden: Die proteinbasierte Vakzine Nuvaxovid hat jetzt die Zulassungsempfehlung erhalten.
Veröffentlicht: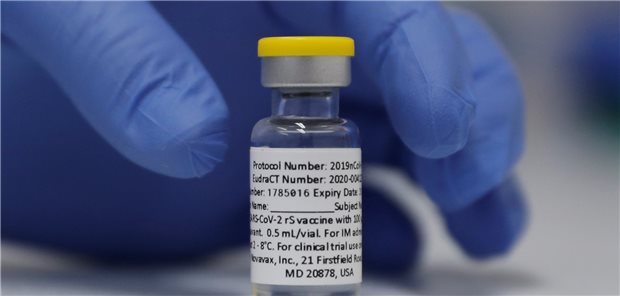
Könnte schon bald in der EU für die Versorgung zur Verfügung stehen: der COVID-19-Impfstoff Nuvaxovid (NVX-CoV2373) von Novavax – hier ein früher Schnappschuss aus einer klinischen Studie Anfang Oktober 2020.
© Alastair Grant / AP Photo / picture alliance
Amsterdam. Erstmals wird in der EU ein Corona-Impfstoff eine Zulassung erhalten, der weder auf einem Vektor noch der mRNA-Technologie basiert. Am Montag votierte der Humanarzneiausschuss CHMP der Europäischen Arzneimittelagentur EMA für eine bedingte Zulassung der proteinbasierten Vakzine Nuvaxovid (NVX-CoV2373) von Novavax. Formal erteilt die Zulassung die EU-Kommission.
Corona-Splitter der KW 48/2021
Welcher Booster wirkt am besten?
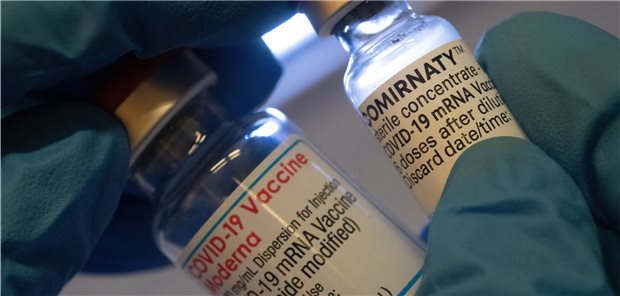
Der rekombinante Impfstoff enthält virusähnliche Partikel, die das SARS-CoV-2-Spike-Protein präsentieren. Die Partikel liegen mit dem sogenannten Matrix-M1™-Adjuvans in Nanopartikeln vor. Das saponin-basierte Adjuvans soll nach Novavax-Angaben die Aktivität antigenpräsentierender Zellen am Injektionsort stimulieren. Den Zulassungsantrag hatte Novavax Mitte November gestellt.
Vorteil in der Versorgung: Nuvaxovid wird als gebrauchsfertige Flüssigformulierung in Mehrdosisfläschchen mit je 10 Impfdosen ausgeliefert. Er wird bei 2°C bis 8°C gelagert. Verimpft werden zwei Dosen je 0,5 ml (50 µg Protein plus 5 µg Adjuvans) im Abstand von 21 Tagen.
In der klinischen Phase-III-Studie PREVENT-19 mit knapp 30.000 Probanden erreichte die Vakzine eine Effektivität von relativ 90,4 Prozent beim klinischen Endpunkt einer COVID-19-Erkrankung. Binnen drei Monaten Follow-up erkrankten 14 von 19.714 Verum-Probanden (absolutes Risiko, AR: 0,07 Prozent) und 63 von 9868, die Placebo erhielten (AR: 0,64 Prozent).
Schwere COVID-19-Fälle traten nur unter Placebo auf (0 vs. 4 Fälle). Allerdings gingen die meisten Fälle in der Studie auf die Alpha-Variante zurück (NEJM online; 15. Dezember). (nös)