Ermutigendes zu Immuntoleranz gegenüber Spenderorganen
Bei weniger als zehn Prozent der Nierenempfänger und bei etwa 20 Prozent der Patienten mit einer fremden Leber entwickelt sich eine Immuntoleranz gegen das Spenderorgan. Ärzte versuchen, sie gezielt zu induzieren.
Veröffentlicht: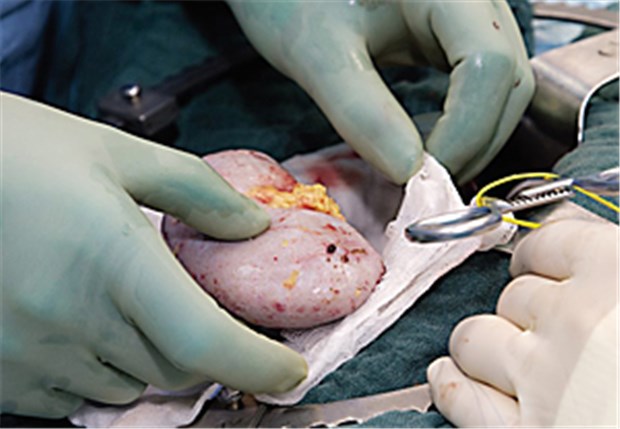
Vorbereitung zur Nierentransplantation.
© horizont21 / fotolia.com
VANCOUVER. Lisa R. ist Mitte vierzig und lebt im US-Bundesstaat Colorado. Als ihre Nieren im Jahr 1996 auf Grund einer Wegenerschen Granulomatose versagten, spendete ihr die Schwester ein Organ. Drei Jahre später leidet sie massiv unter den Folgen der Immunsuppression: sie hat ein Cushing-Syndrom und schwere Depressionen. Außerdem steigt der Kreatinin-Wert und damit das Risiko für einen Transplantatverlust.
Die Patientin tut etwas, wovor Ärzte dringend warnen: Sie schleicht die Medikamente aus. Und Lisa hat großes Glück. Sie ist eine der wenigen Organempfänger, die eine Immuntoleranz gegenüber dem Transplantat entwickelt haben. Auf deutlich unter zehn Prozent wird dieser Anteil unter Nierenempfängern geschätzt, auf etwa 20 Prozent bei Patienten nach einer Lebertransplantation.
Stabile Organfunktion ohne Immunsuppression
Ein Ziel der Arbeiten im Immune Tolerance Network (ITN), eines 1999 von den National Institutes of Health (NIH) gegründeten Forschungskonsortiums: Mit Hilfe von Biomarkern soll es möglich werden, Patienten wie Lisa zu finden, die komplett oder partiell immuntolerant für das Transplantat sind, um Medikamente ausschleichen oder reduzieren zu können.
So korreliert zum Beispiel einer vom ITN geförderten Studie mit 25 transplantattoleranten Nierenempfängern zu Folge eine hohe Expression von drei B-Zell-assoziierten Genen zuverlässig mit einer Immuntoleranz (positiver prädiktiver Wert fast 100 Prozent; JCI 2010; 120: 1836).
Als immuntolerant wurden Transplantatempfänger bezeichnet, die mindestens ein Jahr lang ohne immunsuppressive Therapie eine stabile Organfunktion hatten, ohne Zeichen gewebezerstörender Immunreaktionen. Die Definition ist durchaus gängig, entsprechende Organempfänger zu finden ist allerdings schwierig.
Auch für klinische Studien, bei denen eine Immuntoleranz überhaupt erst induziert werden soll, sind die Hürden hoch. "Einzig das NIH finanziert solche Studien in den USA", so Professor David Sachs von der Harvard Medical School in Boston in Massachusetts beim Kongress der Transplantation Society in Vancouver.
"Es gibt große Probleme, die Risiken der Teilnehmer zu versichern, denn das Ausschleichen oder der Verzicht auf eine Erhaltungstherapie ist schließlich kein Standard", erläuterte Sachs im Gespräch mit der "Ärzte Zeitung". In Frage kommen nur Patienten mit schweren Unverträglichkeiten der Immunsuppression und hohen Risiken, etwa Hautkrebs in der Anamnese.
Und es muss einen starken Wunsch nach Absetzen der Arzneien geben. Ein gutes Monitoring, das Abstoßungen früh anzeigt oder aber die gewünschte, friedliche Koexistenz zwischen Spenderorgan und Empfänger, sei extrem wichtig.
Trotz der Probleme gibt es aktuelle Studien mit ermutigenden Ergebnissen. Ein vom Team um Sachs entwickelter Ansatz ist, den Empfänger vor der Transplantation zu konditionieren durch Inaktivierung, Depletion und Hemmer der Neubildung von immunreaktiven Zellen, und zwar mit Antikörpern gegen CD20 und CD2, Cyclophosphamid und Radiatio des lymphatischen Systems.
Mit dem Nierentransplantat zusammen erhalten die Patienten dann Spenderknochenmark. Zeitgleich wird eine immunsuppressive Therapie begonnen und nach einigen Monaten ausgeschlichen. 5 von 15 geplanten Patienten, die einen nicht-HLA-identischen Lebendspender hatten, sind zwischen Januar und Oktober 2009 so behandelt worden.
Vier haben nach Ausschleichen der Immunsuppression eine stabile Nierenfunktion mit Kreatininwerten im Normbereich, ohne Bildung von HLA-Antikörpern.
Stammzellen werden Empfängern infundiert
Das Team um Professor Samuel Strober von der Stanford University beginnt mit der Therapie erst am Tag der Transplantation: Anti-Thymozyten-Globulin (ATG, für 5 Tage), Prednisolon (10 Tage) und eine fraktionierte Bestrahlung des lymphatischen Gewebes werden gefolgt von der Infusion CD34- und CD3-angereicherter Stammzellen aus dem Spenderblut.
Die Erhaltungsimmunsuppression wird ausgeschlichen, wenn sich beim Empfänger ein geringer, aber konstanter Anteil von Spenderzellen über mindestens sechs Monate nachweisen lässt (Mikrochimärismus). Das war bei 9 von 12 seit 2004 aufgenommenen Patienten der Fall, die alle noch immer eine sehr gute Transplantatfunktion hätten, so Strober. Acht benötigten keine Immunsuppression, bei ihnen gab es auch keine Abstoßungsreaktionen.
Lesen Sie dazu auch: Immunisierung soll Toleranz induzieren




