Acinetobacter baumannii
Problemkeim fordert Klinikpersonal heraus
Ausbrüche mit multiresistenten Keimen namens Acinetobacter baumannii wie jüngst an der Kieler Uniklinik gibt es regelmäßig in Krankenhäusern. Was macht diesen Erreger so gefährlich?
Veröffentlicht: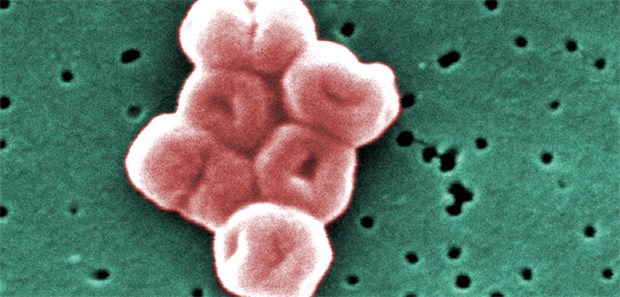
Acinetobacter baumannii: Der Keim beunruhigt Ärzte am Universitätsklinikum Kiel.
© CDC / Matthew J. Arduino
KIEL. Bei dem jüngsten Ausbruch im Universitätsklinikum Schleswig-Holstein (UKSH) in Kiel ist Acinetobacter baumannii bei 31 Patienten nachgewiesen worden.
Zwölf der Patienten sind gestorben, bei dreien könnte nach Auskunft der Ärzte der Keim die Ursache gewesen sein.
Besorgnis erregt besonders die Unempfindlichkeit des Keims in Kiel. Er ist gleich gegen vier Antibiotikagruppen resistent und wird daher den 4MRGN (multiresistente gramnegative Erreger) zugeordnet.
Resistenzen gibt es gegen Acylureidopenicilline, Cephalosporine der dritten und vierten Generation, Fluorchinolone und Carbapeneme.
In der Praxis bedeutet das, dass gängige Therapien mit Piperacillin oder Tazobactam, Cefotaxim oder Ceftazidim, Ciprofloxacin und sogar Imipenem oder Meropenem nicht mehr wirksam sind.
Allgemein ist in deutschen Kliniken der Anteil solcher 4MRGN bei A. baumannii von 6,4 Prozent 2008 auf 13,6 Prozent 2011 gestiegen.
Auf Intensivstationen lag ihr Anteil 2012 bei 19,6 Prozent (Epi Bul 2014; 21: 183). In anderen Ländern wie Griechenland oder Mexiko sind bereits mehr als 50 Prozent der Stämme resistent gegenüber Carbapenemen.
Mittlerweile wird aus anderen Ländern sogar über panresistente Stämme berichtet, die auch unempfindlich gegen die Reserve-Antibiotika Tigecyclin und Colistin sind. A. baumannii ist zudem offenbar ein "genetischer Schmelztiegel", der Resistenzgene aufnimmt, rekombiniert und die brisanten Eigenschaften an andere Bakterien wie Klebsiella oder E. coli weitergibt.
Kein harmloser Umweltkeim
Acinetobacter-Species kommen im Wasser, im Boden, auf Pflanzen, als natürliche Flora auf der Haut von Mensch und Tier, aber auch in Parasiten und Insekten vor.
Aufgrund ihrer Umweltresistenz und ihrer ausgeprägten Fähigkeit zur Ausbildung von Antibiotikaresistenzen gewinnen sie zunehmende Bedeutung als Erreger nosokomialer Infektionen, allen voran A. baumannii.
Weitere hierzulande klinisch wichtige Spezies sind A. pittii und A. nosocomialis.A. baumannii ist alles andere als ein harmloser Umweltkeim. Sein primäres Reservoir ist zu 90 Prozent der kolonisierte Mensch, betont Professor Harald Seifert vom Institut für Mikrobiologie, Immunologie und Hygiene der Universität Köln.
In Kliniken wird der Keim meist über einen besiedelten Patienten eingeschleppt. Aber auch bei chronischen Atemwegsinfekten können die Keime verbreitet werden. Dabei hat sich der Erreger bestens an Kliniken angepasst.
Er bewegt sich auf feuchten Oberflächen schnell fort, bildet Biofilme und kann ausgetrocknet wochenlang auf Oberflächen überleben, etwa in Beatmungsgeräten, auf Computertastaturen oder Telefonen.
Die Übertragung von Patient zu Patient erfolgt meist durch die Hände des Klinikpersonals, über kontaminierte Oberflächen und medizinische Geräte.
Möglicherweise kann A. baumannii auch über die Luft übertragen werden. Das Übertragungspotenzial übersteigt das von Methicillin-resistenten Staph. aureus (MRSA) deutlich (Epi Bull 2013; 32: 295).
Risikofaktoren für eine Besiedelung oder Infektion mit multiresistenten A. baumannii sind längere stationäre Behandlung, Aufenthalt auf der Intensivstation, Beatmung, antibiotische Vorbehandlung, vorausgehende invasive Maßnahmen sowie schwere Grunderkrankungen.
Man geht davon aus, dass sich bei 20 bis 55 Prozent der besiedelten Patienten in der Klinik eine Infektion manifestiert. Bei schwer kranken Patienten mit abgeschwächter Immunabwehr kann es dabei zu Wundinfektionen, Bakteriämie, Sepsis, Pneumonie, Meningitis oder Harnwegsinfektionen kommen.
Die Sterberaten vor allem bei Septikämien mit Carbapenem-resistenten Stämmen betragen zum Teil über 40 Prozent. Mittlerweile werden weltweit neun Prozent aller Infektionen auf Intensivstationen durch Acinetobacter spp. verursacht, besonders hoch (17 bis 19 Prozent) sind die Infektionsquoten mit A. baumannii in Osteuropa und Asien.
In Deutschland liegt die Prävalenz für Acinetobacter bei Pneumonien auf Intensivstationen bei etwa zwei Prozent. Bei Ausbrüchen mit A. baumannii wurden im Mittel fünf Patienten pro Monat neu mit dem Erreger besiedelt.
Bekannt wurde A. baumannii vor allem durch seinen Nachweis in infizierten Wunden von US-Soldaten, die aus Einsätzen im Irak und Afghanistan zurückkamen. Über 30 Prozent der Wunden waren mit dem Keim infiziert.
Erweiterte Vorsichtsmaßnahmen
"Hygienemaßnahmen bei Infektionen oder Besiedelung mit multiresistenten gramnegativen Stäbchen" hat die Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) des RKI zusammengestellt (Bundesgesundheitsbl 2012; 55: 1311).
Alle mit 4MRGN A. baumannii besiedelte oder infizierte Patienten sind danach zu isolieren und Flächen in der Patientenumgebung mit häufigem Hände- und Hautkontakt sowie Fußböden täglich zu desinfizieren.
Zudem rät die KRINKO dazu, alle Patienten mit Risiko für eine Besiedelung zu screenen und bis zum Vorliegen der Ergebnisse zu isolieren. Dabei sollen die Kliniken eigene regionale Richtlinien erstellen, welche Patienten einem Screening unterzogen werden.
Empfohlen wird inzwischen, alle Patienten nach einem Aufenthalt in einer Klinik im Ausland zu screenen sowie Patienten, die in den vergangenen zwölf Monaten mehr als drei Tage in einer Region mit erhöhter 4MRGN-Prävalenz in Deutschland stationär behandelt wurden.
Außer Abstrichen aus dem Mund-Rachen-Raum sollten möglichst großflächige Proben von der Haut genommen werden. Ob die antiseptische Ganzkörperwaschung zur Eradikation effektiv ist, ist unklar .
Der Präsident der Deutschen Gesellschaft für Hygiene und Mikrobiologie (DGHM), Professor Mathias Hermann, entlastet in einer Stellungnahme die Ärzte des Kieler Klinikums.
Trotz konsequenter Einhaltung von Hygienemaßnahmen nach Keimnachweis sei das Risiko einer Erregerübertragung nicht völlig auszuschließen.
Er sehe "aktuell keinen Anlass für Schuldzuweisungen oder überzogene, durch wissenschaftliche Erkenntnisse nicht belegte "Hygiene-Forderungen".