Retinopathie: Wann ist der HbA1c relevant?
So manche aktuelle Erkenntnis zur diabetischen Retinopathie ist auch für den diabetologischen Alltag interessant. Darauf hat Professor Hans-Peter Hammes aus Mannheim bei einer Veranstaltung in Mainz aufmerksam gemacht.
Veröffentlicht:MAINZ. Klinisch werden bei der diabetischen Retinopathie nicht proliferative von proliferativen Stadien unterschieden. Zu den frühen Veränderungen der nicht proliferativen Erkrankung gehören Mikroaneurysmen, Aussackungen der Kapillarwände, im Verlauf können Blutungen, harte Exsudate, Cotton-Wool-Herde, mikrovaskuläre Anomalien und venöse Kaliberschwankungen (Perlschnurvenen) hinzukommen.
Die proliferative diabetische Retinopathie, die den Visus akut bedrohen kann, ist gekennzeichnet durch präretinale Neovaskularisationen und Einblutungen, Glaskörperblutungen, Gefäßeinsprossung in die Iris (Rubeosis iridis) und Winkelblockglaukome, im Spätstadium droht die Retinaablösung.
Das diabetische Makulaödem kann in jedem Stadium auftreten.Zu den Risikofaktoren für die Entstehung einer Retinopathie zählen v.a. die Diabetesdauer und ein erhöhtes HbA1c, für die Progression zu schweren Formen auch die Hypertonie. Typ-1-Diabetiker haben generell ein höheres Risiko als Typ-2-Diabetiker.
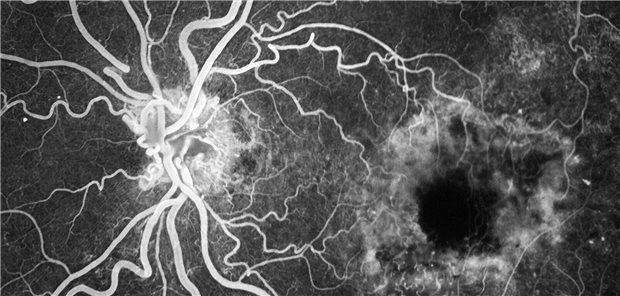
Zur Prävalenz der Retinopathie gab es lange nur unzureichende Angaben. Mit der Fundusfotografie habe sich das geändert, so Hammes. Weltweit geht man nun von einer Gesamtprävalenz von 35% aus.
Einer aktuellen Metaanalyse zufolge sind ca. 7% der Weltbevölkerung von proliferativer diabetischer Retinopathie betroffen, ca. 7,5% von einem diabetischen Makulaödem, und bei ca. 12% ist der Visus durch eine Retinopathie bedroht.
Inzidenz-Daten für Deutschland
An absoluten Zahlen ergeben sich daraus 17,2 Mio. Patienten mit proliferativer diabetischer Retinopathie und 28,4 Mio. mit durch Retinopathie gefährdetem Visus.
Neue Daten für Deutschland liefert das Register zur Diabetes-Patienten-Verlaufsdokumentation (DPV), und zwar für Typ-1- und Typ-2-Diabetiker. Erfreulich: "In Deutschland liegt die kumulative Inzidenz der diabetischen Retinopathie mit 27-29% niedriger als weltweit betrachtet", so Hammes.
Für das diabetische Makulaödem gebe es keine Daten bei Typ-1-Diabetes (T1D). Bei Typ-2-Diabetes (T2D) sei es mit 0,8% Prävalenz in Deutschland sehr selten — ein wichtiger Aspekt im Hinblick auf die Therapiekosten.
Die Inzidenz der schweren nicht proliferativen und der proliferativen diabetischen Retinopathie nimmt ab, darauf deuten finnische Daten hin. Ein Grund dafür könnte laut Hammes das verbesserte Screening mit konsekutiv früherer Therapie sein.
Insgesamt allerdings nimmt die Prävalenz von Visuseinschränkungen zumindest in den USA zu. Dies könnte am ehesten an den steigenden Diabetikerzahlen liegen.
Fehlende Progression gutes Omen
Ein Teil der Typ-1-Diabetiker lebt mehr als 50 Jahre mit einer Insulintherapie und entwickelt keine proliferative Retinopathie. Woran das liegen könnte, wurde in einer US-Studie geprüft: Die Teilnehmer waren im Mittel 67 Jahre alt und hatten den Diabetes im Mittel mit 11 Jahren bekommen.
Nur die Hälfte der zunächst analysierten 350 Langzeitdiabetiker erkrankte an einer proliferativen Retinopathie. Eine gute Blutzuckerkontrolle war dabei nicht entscheidend, eher ein günstiges Lipidprofil.
Der HbA1c-Wert ist laut Hammes ab einem bestimmten Zeitpunkt im Diabetesverlauf für die Retinopathieprogression nicht mehr relevant. Daher sei eine proliferative Retinopathie allein keine Indikation für eine intensive Diabetestherapie.
Unabhängig von Risikofaktoren wurde beobachtet: Hatte sich eine Retinopathie innerhalb der ersten 17 Jahre des Follow-up nicht verschlimmert, tat sie es auch in 96% der Fälle später nicht mehr.
Hammes: "Wird im Screening eine proliferative Retinopathie festgestellt, die durch eine Lasertherapie zur Ruhe kommt, dann ist die Prognose gut." Diesen Patienten könnten weitere aggressive Maßnahmen erspart bleiben.
In frühen Retinopathiestadien allerdings ist eine schlechte Blutzuckereinstellung ein Risiko für das Auge. Wie nun belegt werden konnte, spricht das häufige Entstehen und (Pseudo-)Verschwinden von Mikroaneurysmen in der Nähe der Makula — ähnlich wie ein erhöhter HbA1c-Wert — ebenfalls für ein hohes Makulaödem-Risiko.
Blutdruck oder Visus hatten in der entsprechenden Studie, an der Typ-2-Diabetiker mit milder nicht proliferativer Retinopathie teilgenommen hatten, keinen prädiktiven Wert, so Hammes.
Die Mikroaneurysmen-Dynamik ist allerdings nur über die Fundusfotografie und eine gute Dokumentation feststellbar. Daher könnten diese Verlaufsuntersuchungen für die Patientenselektion zur intravitrealen operativen Medikamentengabe (IVOM) nützlich sein. Wichtig sei es auch, vom Augenarzt die genaue Lage von Mikroaneurysmen zu erfragen, sagte Hammes.
Schon länger ist bekannt, dass Patienten mit fortgeschrittener Retinopathie eine erhöhte kardiovaskuläre Mortalität haben. Ob sich das bei einer Retinopathie früher Stadien ebenso verhielt war unklar. Der Beweis ist laut Hammes sowohl bei T1D als auch T2D jetzt erbracht: "Schon wer Mikroaneurysmen entwickelt, hat ein erhöhtes kardiovaskuläres Risiko."
Betroffene benötigen besondere Aufmerksamkeit. Mikroaneurysmen seien der wichtigste kardiovaskuläre Biomarker nach der Mikroalbuminurie. Er lieferte damit ein weiteres Argument für eine regelmäßige Fundusdiagnostik bereits früh im Diabetesverlauf.
Die okulo-nephrologische AssoziationOb ein Patient mit Niereninsuffizienz eine Proteinurie hat oder nicht, ist auch mit Blick auf die Augen wichtig. Denn seit dieser Studie ist klar: Die Patienten unterscheiden sich im Retinopathierisiko. "Niereninsuffizienzpatienten mit einer Proteinurie entwickeln häufiger eine Retinopathie als die ohne", sagte Hammes.
Das gelte auch für Nichtdiabetiker. Umgekehrt ist ebenfalls erhöhte Aufmerksamkeit gefragt: Ein klinisch signifikantes Makulaödem oder eine proliferative diabetische Retinopathie sind laut Hammes mit einer verstärkten Nierenschädigung assoziiert.
Daher: "Wann immer ein Befund kommt ‘der Patient hat was am Auge' auch auf die Nieren gucken!"