Clostridium difficile
Wie Sporen vor Rückfällen schützen
Wer eine Infektion mit Clostridium difficile überstanden hat, ist nicht vor einem Rückfall gefeit. Doch mit der Gabe von Sporen lässt sich davor offenbar schützen.
Veröffentlicht: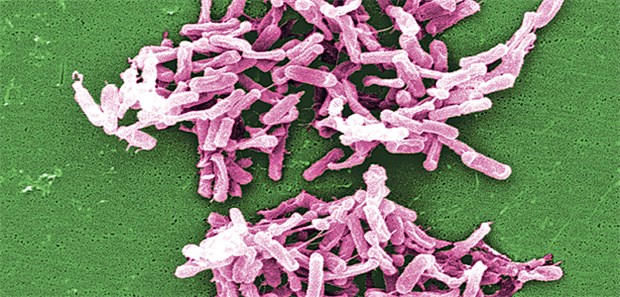
In Kliniken gefürchtet: Clostridium difficile aus einer Stuhlprobe unter dem Mikroskop. Nicht-toxigene Stämme des Keims werden jetzt in klinischen Studien zur Rezidivprophylaxe der Infektionen getestet.
© Janice Haney Carr / CDC
HINES. Bei gut jeder vierten Infektion mit Clostridium difficile (CDI) gibt es Rezidive. Einen gewissen Schutz davor bietet nach Studiendaten die gastrointestinale Besiedelung mit nicht-toxigenen C. difficile (NTCD).
Die optimale Dosis und die Sicherheit einer oralen Therapie mit Sporen von NTCD wurde jetzt in einer Phase-II-Studie mit 173 erwachsenen Patienten untersucht, berichten Forscher um Dr. Dale Gerding vom Edward Hines Jr VA Hospital in Hines im US-Staat Illinois (JAMA 2015; 313: 1719).
Die Patienten kamen aus 44 Studienzentren in den USA, Kanada und Europa und waren erfolgreich gegen CDI mit Metronidazol und/oder Vancomycin therapiert worden.
Zur Rezidiv-Prophylaxe bekamen sie dann in drei Gruppen eine flüssige Zubereitung von Sporen des NTCD-Stamms M3, und zwar entweder über sieben Tage 104 oder 107 Sporen pro Tag oder über 14 Tage 107 Sporen/Tag. Eine Kontrollgruppe erhielt über 14 Tage Placebo.
Außer Sicherheit und Akzeptanz der oralen Clostridienbehandlung wurden die Kolonisationsraten bis zu sechs Wochen nach der Therapie sowie die CDI-Rezidivraten über sechs Wochen erhoben. Insgesamt wurden die Probanden 26 Wochen nachbeobachtet.
Niedrigste Rückfallquote 5 Prozent
Von den 168 Probanden beendeten 157 die Therapie. Bei 69 Prozent der Teilnehmer, die mit NTCD-M3 behandelt wurden, kam es zu einer Kolonisation im Gastrointestinaltrakt, die mit der Zeit allerdings zurückging. Nach 22 Wochen war NTCD-M3 nicht mehr im Stuhl nachweisbar.
Ein CDI-Rezidiv erlitten 30 Prozent der Probanden der Placebogruppe und 11 Prozent aller Patienten mit NTCD-M3 (Odds Ratio, OR 0,28). Die niedrigste Rückfallquote wurde mit der am höchsten konzentrierten Sporensuspension erreicht (5 Prozent bei 107 Sporen/d über sieben Tage).
In der Gruppe, die 14 Tage mit 107 Sporen/d behandelt wurden, lag die Rezidivquote bei 15 Prozent. Voraussetzung für den Schutz vor einer erneuten Infektion war die Ansiedelung der Bakterien im Darm.
Von den nach NTCD-M3-Behandlung kolonisierten Patienten erlitten nur zwei Prozent ein Rezidiv. Hatten sich die NTCD-M3 dagegen nicht angesiedelt, lag die Rückfallquote bei 31 Prozent.
78 Prozent der Patienten unter NTCD-M3 und 86 Prozent in der Placebogruppe, klagten über mindestens eine therapiebedingte Nebenwirkung. Zum Beispiel traten Diarrhö und Bauchschmerzen sowohl in den Verum- als auch in der Placebogruppe auf (unter NTCD-M3: 46 und 17 Prozent; unter Placebo 60 und 33 Prozent).
Höhere Rezidivrate sollte untersucht werden
Schwere Nebenwirkungen ereigneten sich bei 3 Prozent der Probanden unter NTCD-M3 und bei 7 Prozent unter Placebo. Keine dieser Ereignisse konnte jedoch mit der Behandlung in Zusammenhang gebracht werden.
Im Vergleich zu Placebo erwies sich die Behandlung mit NTCD-M3 als sicher und gut verträglich.
Die höhere Rezidivrate bei 14-tägiger Behandlung, so die Autoren, müsse in weiteren Studien untersucht werden. Wie der CDI-Schutz durch den nicht-toxigenen Stamm funktioniere, sei im Einzelnen noch nicht bekannt.
Die wahrscheinlichste Hypothese sei, so Gerding und Kollegen, dass NTCD-M3 und toxigene CD um die gleichen Stoffwechselwege oder Anheftungsorte im Gastrointestinaltrakt konkurrieren.
Sei NTCD-M3 einmal angesiedelt, mache er seine Nische möglicherweise nicht mehr so schnell für toxigene Eindringlinge frei. Wichtig sei dabei aber, dass toxigene C.-difficile zuvor durch die spezifische Antibiotikatherapie vollständig eliminiert würden, um eine Übertragung von Toxingenen auf den nicht-toxigenen Stamm auszuschließen.
Antitoxin wird entwickelt
Einen längeren Schutz als die orale Behandlung mit NTCD-M3 könnte möglicherweise ein injizierbares Antitoxin bieten, das sich derzeit in der klinischen Entwicklung befindet.
Allerdings würden insbesondere bei alten Menschen Wochen bis Monate vergehen, bis dieses voll wirksam sei. Die Zeit, bis ausreichend viele Antikörper vorlägen, so die Forscher, könnte dann zum Beispiel mit NTCD-M3 überbrückt werden.