COVID-19-Vakzine
Auch BioNTech beantragt EMA-Zulassung für Corona-Impfstoff
Fast zeitgleich mit Moderna haben BioNTech und Pfizer für ihren gemeinsam entwickelten Corona-Impfstoffkandidaten eine EMA-Zulassung beantragt. Die deutsch-amerikanischen Partner bereiten in weiteren Ländern den Zulassungsantrag vor.
Veröffentlicht:
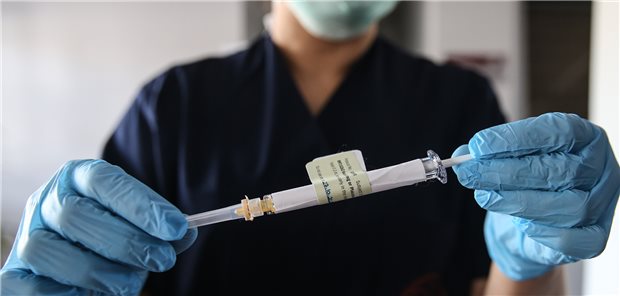
Beim Wirkstoff BNT162b2 von BioNTech und seinem Entwicklungspartner Pfizer handelt es sich um einen mRNA-Kandidaten. (Symbolbild)
© Zeljko Lukunic / PIXSELL / picture alliance
Mainz und New York. BioNTech und Pfizer haben eine Zulassung für ihren gemeinsam entwickelten Corona-Impfstoffkandidaten BNT162b2 bei der Europäischen Arzneimittelbehörde EMA beantragt. Das schreibt BioNTech auf seiner Webseite.
Die EMA habe den Antrag auf bedingte Marktzulassung, der bereits am Montag erfolgt sein soll, bestätigt. Damit hätten BioNTech und Pfizer fast zeitgleich den EMA-Antrag mit Moderna eingereicht. Das US-Unternehmen hatte am Montag angekündigt, noch am selben Tag die EMA-Zulassung und eine Notfallzulassung bei der amerikanischen Behörde FDA zu beantragen. Die FDA-Zulassung hatten BioNTech und Pfizer bereits vor einiger Zeit beantragt. Zugleich initierten die Unternehmen rollierende Zulassungen in Australien, Kanada und Japan, hieß es.
BioNTech und Pfizer wollen im Falle erfolgreicher Zulassungen die globale Verteilung ihrer COVID-19-Vakzine ermöglichen, schreiben sie in ihrer gemeinsamen Pressemitteilung. „Hiermit möchten wir zu den globalen Bemühungen bei der Bekämpfung des Virus beitragen, um wieder zu einem Normalzustand zurückzukehren“, so BioNTech-Mitgründer und CEO Prof. Ugur Sahin weiter.
Corona-Impfstoff
BioNTech gibt in Sachen Impfstoff-Kühlung Entwarnung
Die Kooperationspartner verweisen dabei noch einmal auf die Ergebnisse ihrer Phase-III-Studie für den Imfstoffkandidaten BNT162b2 mit fast 44.000 Teilnehmern: In dieser Studie lag der Impfsschutz bei 95 Prozent, sieben Tage nach Gabe der zweiten Impfdosis. Bei Älteren über 65 Jahren lag der Schutz demnach bei 94 Prozent. Die Vakzine sei zudem gut verträglich und bisher ohne schwere Nebenwirkungen gewesen. (ajo)
Neueste Entwicklungen: Die Europäische Arzneimittel-Agentur EMA will noch im Dezember über eine Zulassungsempfehlung für den Corona-Impfstoff der Mainzer Firma BioNTech und des US-Pharmakonzerns Pfizer entscheiden. Bis spätestens 29. Dezember soll ein Ergebnis der Prüfung vorliegen, teilte die Agentur am Dienstag in Amsterdam mit. Zum Antrag des US-Konzerns Moderna auf Zulassung seines Impfstoffs werde eine Entscheidung bis zum 12. Januar erwartet. BioNTech/Pfizer und Moderna hatten ihre Anträge auf Zulassung für die EU am Montag eingereicht. Sollte die EMA grünes Licht geben, kann die EU-Kommission die Verwendung der Impfstoffe für alle Mitgliedsländer genehmigen. Die Kommission folgt in der Regel der EMA-Empfehlung.
Unterdessen hat Bundesforschungsministerin Anja Karliczek (CDU) erneut um Vertrauen im Zusammenhang mit der schnellen Entwicklung von Corona-Impfstoffen geworben. Bei aller Geschwindigkeit blieben die Prüfungsmaßstäbe auf dem hohen Niveau, das auch sonst bei der Zulassung von Impfstoffen angelegt werde, sagte sie am Dienstag in Berlin. „Ein Covid-19-Impfstoff muss sicher und wirksam sein – so wie jeder andere Impfstoff auch.“
Karliczek kündigte eine Informationskampagne an: Die Bundesregierung werde alles unternehmen, um die Bürger über die Vorteile der Impfung aufzuklären – aber auch über mögliche Nebenwirkungen. „Und um es noch einmal deutlich zu sagen: Die Impfung bleibt freiwillig. Wer sich impfen lässt, schützt sich aber nicht nur selbst, sondern tut auch etwas für die Gemeinschaft“, fügte die Ministerin hinzu. Impfen zu können, sei eine der größten Errungenschaften der Gesundheitsforschung. (dpa)