Überzeugen Sie sich von den Trulicity®-Vorteilen
Der Trulicity®-Fertigpen injiziert auf Knopfdruck über eine nichtsichtbare Nadel die jeweils enthaltene Dosis von 1,5 mg oder 0,75 mg Dulaglutid.1
Seine einfache und patientenfreundliche Anwendung wurde in einer Studie6 belegt: Mehr als 96 % der Teilnehmer fanden den Gebrauch des Fertigpens als einfach und wollten ihn weiterhin nutzen.6
Zusätzlich ermöglicht die nur 1 x wöchentlich und dabei Mahlzeiten unabhängige Anwendung den Patienten eine höhere Flexibilität in ihrem Alltag.

Ein kurzes Video erklärt Ihnen in nur 47 Sekunden Schritt für Schritt die wichtigsten Punkte zur korrekten Handhabung des Trulicity®-Fertigpens.2
Eine Therapie mit GLP-1-RA wie Trulicity® sollte am Punkt der 1. Injektion vor einer Insulintherapie in Betracht gezogen werden.3
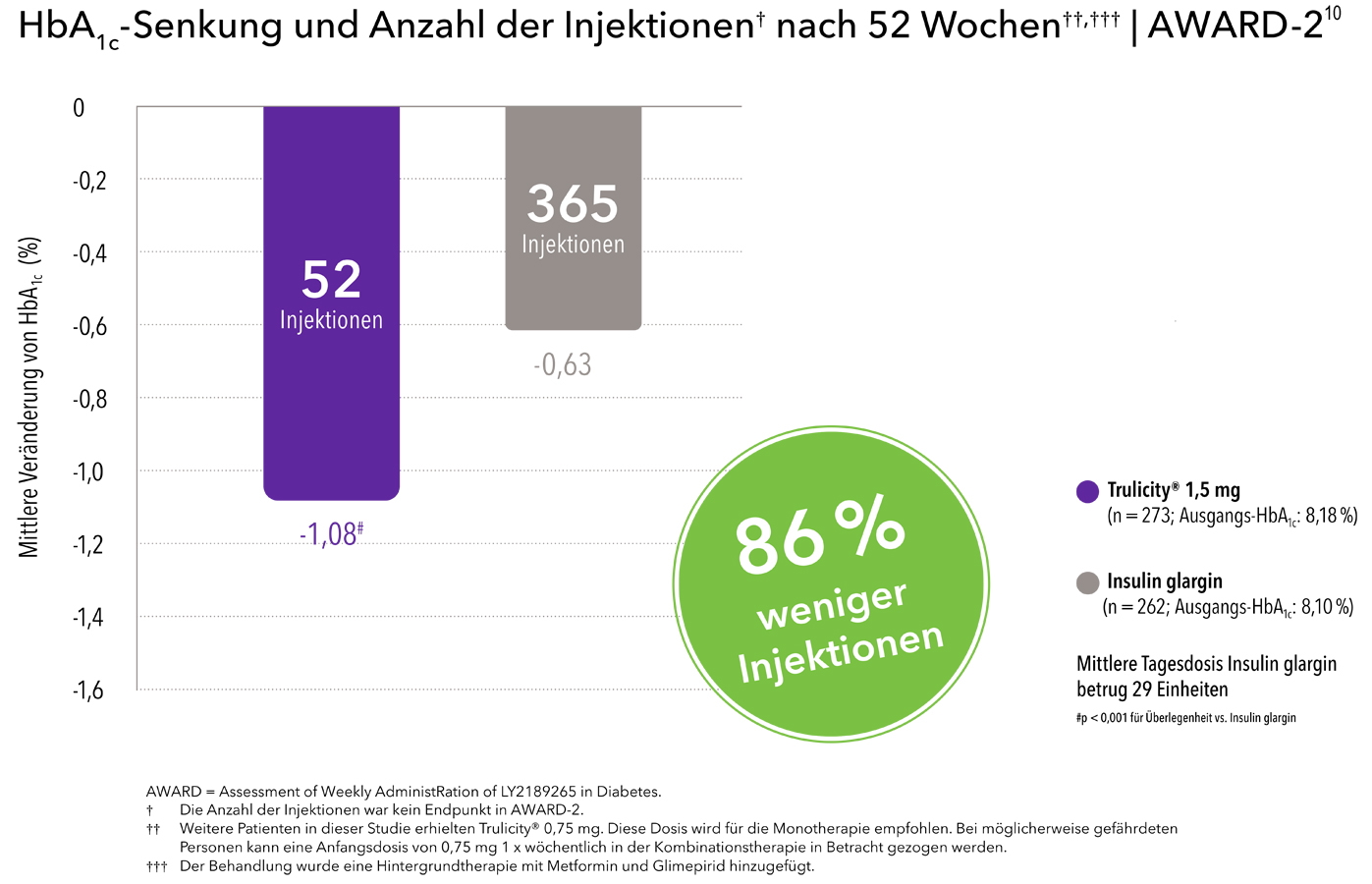
Zwei Post-hoc Analysen bestätigen die Vorteile von Trulicity® hinsichtlich der HbA1C-Kontrolle gegenüber einer Therapie mit Insulin glargin.4,5 Zusätzlich sind unter Trulicity® bis zu 86 % weniger Injektionen erforderlich (siehe Grafik, modifiziert nach Giorgino et al. 201510).
Darüber hinaus kann eine Therapie mit Trulicity® einen günstigen Einfluss auf das Körpergewicht** Ihrer Patienten haben, während es unter einer Insulin-Therapie nicht selten zu einer Gewichtszunahme kommen kann.10
* 8 klinische Phase-III-Studien zeigen eine statistisch überlegene HbA1C-Reduktion für Dulaglutid 1,5 mg im Vergleich zu: Metformin, Sitagliptin, Exenatid zweimal täglich, Insulin glargin und Placebo.1 Zwei weitere Phase-III-Studien zeigten eine statistisch nicht unterlegene HbA1C-Reduktion für Dulaglutid 1,5 mg im Vergleich zu Insulin glargin (jeweils in Kombination mit Insulin lispro) bei Patienten mit Typ-2-Diabetes und mäßiger bis schwerer chronischer Nierenerkrankung (AWARDa-7)1,12 und im Vergleich zu der maximal zugelassenen Dosis von Liraglutid 1,8 mg (AWARD-6).1,13
** Dulaglutid ist nicht angezeigt zur Gewichtsabnahme; die Änderung des Körpergewichts war in den klinischen Studien ein sekundärer Endpunkt.
a) AWARD = Assessment of Weekly AdministRation of LY2189265 (Dulaglutid) in Diabetes
Für die Mehrheit Ihrer Patienten mit Typ-2-Diabetes, bei denen eine Injektionstherapie notwendig wird, kann Trulicity® die richtige Wahl sein.
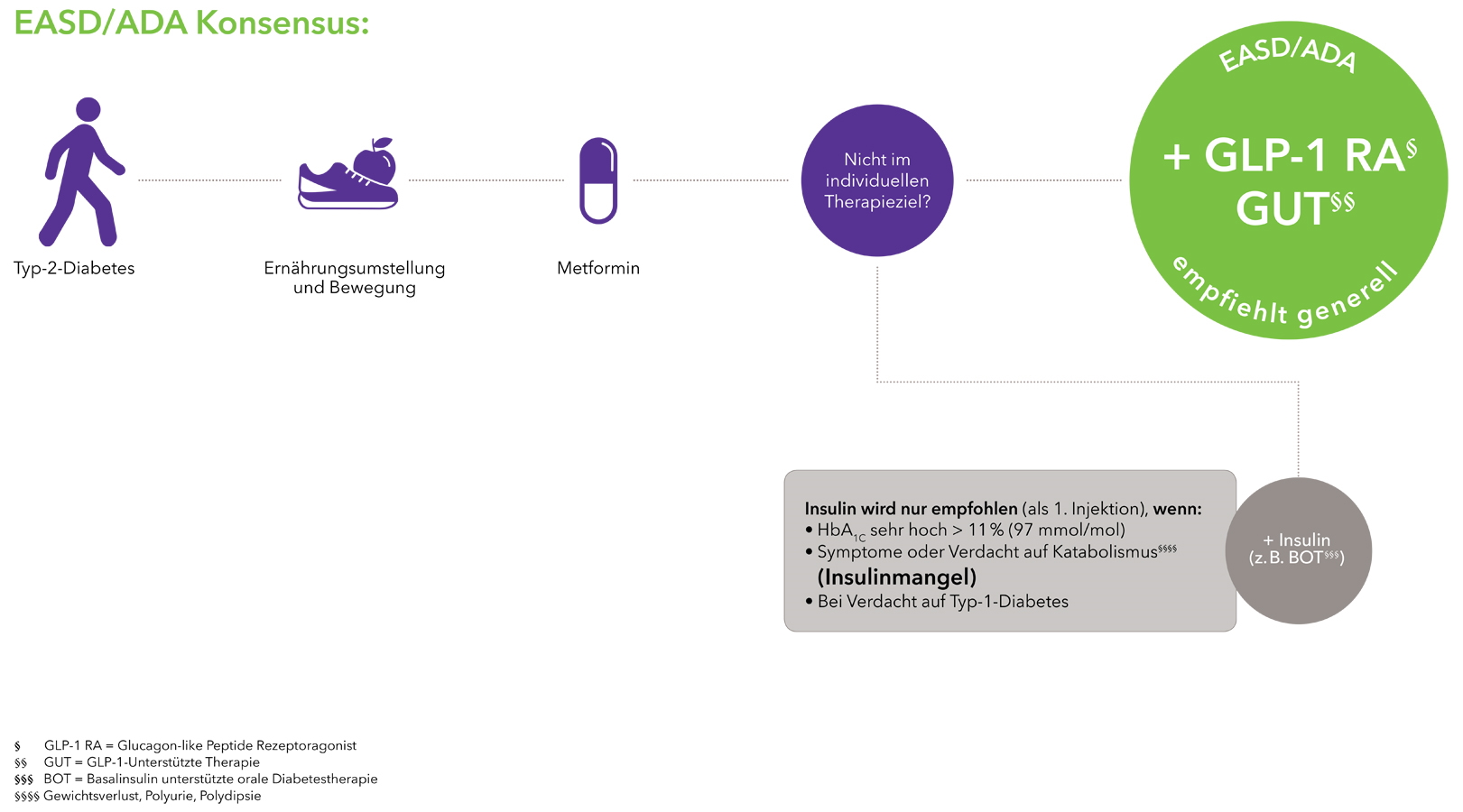
Auch die Fachgesellschaften ADA/EASD empfehlen am Punkt der ersten Injektion einer GLP-1-RA unterstützten Therapie (GUT) den Vorzug gegenüber einer mit Basalinsulin unterstützten oralen Therapie (BOT) zu geben.3

 Prävention kardiovaskulärer Ereignisse+ bei Patienten mit und ohne kardiovaskulärer Vorerkrankung1,++
Prävention kardiovaskulärer Ereignisse+ bei Patienten mit und ohne kardiovaskulärer Vorerkrankung1,++
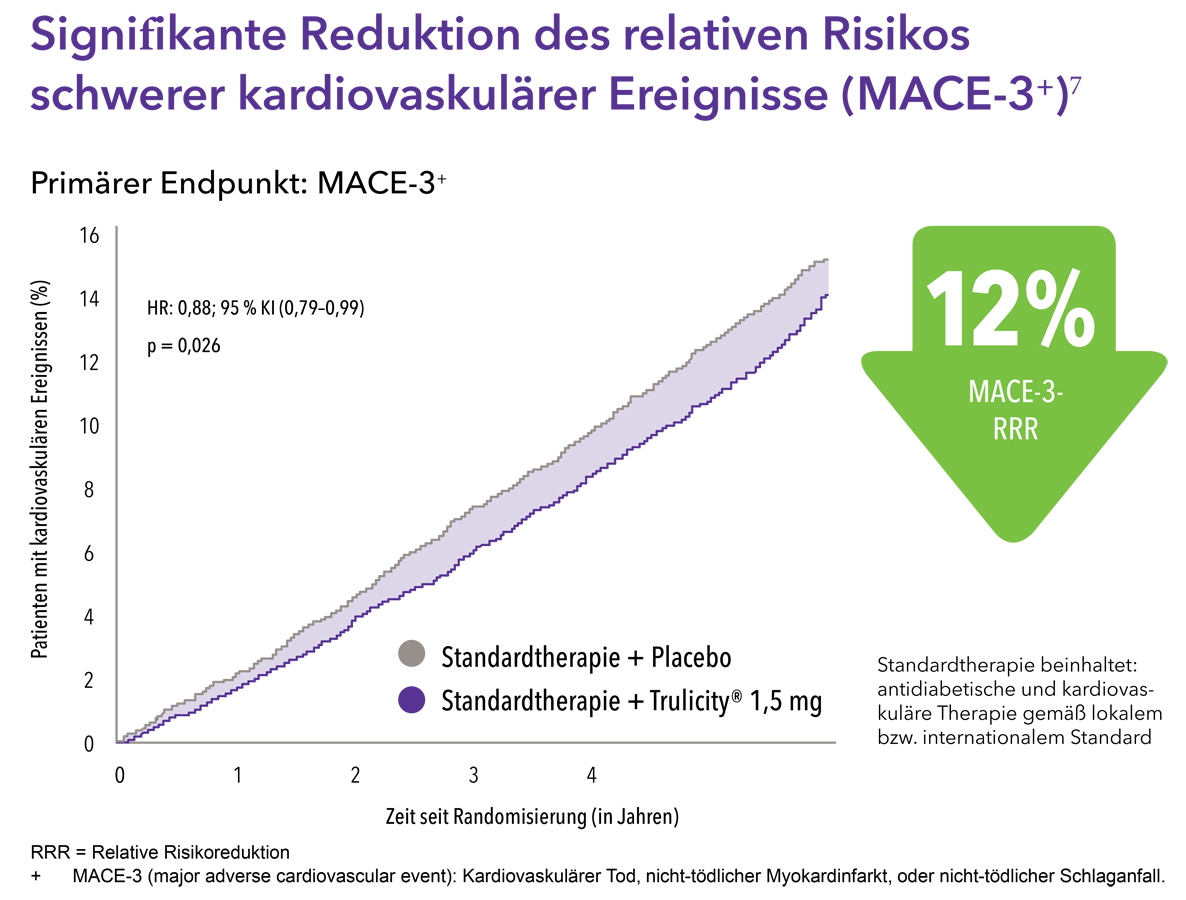
Trulicity® 1,5 mg reduziert signifikant das relative Risiko schwerer kardiovaskulärer Ereignisse (MACE-3+) bei Menschen mit Typ-2-Diabetes.1,7
Trulicity® 1,5 mg ist der erste GLP-1-RA, für den in einer Population mit mehrheitlich Patienten mit Typ-2 Diabetes und kardiovaskulären Risikofaktoren, aber ohne klinisch manifeste CV-Vorerkrankung+++, eine MACE-Prävention+ gezeigt werden konnte.++ Der MACE-Effekt war konsistent über die präspezifizierten Subgruppen.1
+ MACE-3 (major adverse cardiovascular event): Kardiovaskularer Tod, nicht-tödlicher Myokardinfarkt, oder nicht-tödlicher Schlaganfall.
++ Belegt durch eine placebokontrollierte, doppelblinde kardiovaskuläre Langzeit-Outcome-Studie REWIND7,b, bei welcher Patienten mit Typ-2 Diabetes und unterschiedlich hohem kardiovaskulären Risiko (Alter = 50 Jahre und klinisch manifeste Gefäßerkrankung, Alter = 55 Jahre und subklinische Gefäßerkrankung; Alter = 60 Jahre und Zutreffen von mind. 2 weiteren Risikofaktoren)9 Dulaglutid 1,5 mg oder Placebo jeweils in Kombination mit einer Standardtherapie verabreicht wurde.1
+++ 31,5 % der in REWINDb untersuchten Patienten hatten eine klinisch manifeste kardiovaskuläre Vorerkrankung.1
b) REWIND = Researching cardiovascular Events with a Weekly INcretin in Diabetes
Unter Trulicity® ist keine Dosisanpassung bei Patienten mit einer leichten, mäßigen oder schweren Einschränkung der Nierenfunktion (eGFR < 90 bis = 15 ml/min/1,73m2) erforderlich.1
Bei Patienten mit einer terminalen Niereninsuffizienz (< 15 ml/min/1,73 m2) ist die Anwendung von Trulicity® nicht empfohlen.1

Mit Trulicity® können Sie Ihre Patienten noch effizienter schulen. Durch die einfache Anwendung6 des Trulicity®-Fertigpens haben Sie einen geringeren Schulungsaufwand.1
Zusätzlich erfordert eine Therapie mit Trulicity® keine Blutzuckermessungen.1,°
Ein kurzes Video erklärt Ihnen in nur 47 Sekunden Schritt für Schritt die wichtigsten Punkte zur korrekten Handhabung des Trulicity®-Fertigpens.2
In knapp 2,5 Minuten erklärt Ihnen das Video die Wirkweise von Trulicity®.
Beide Videos sind Teil der Trulicity®-Videokarte, einem handlichen Tablet, das ein ideales Hilfsmittel ist um Ihren Patienten die Anwendung und Wirkweise (in 5 Sprachen) von Trulicity® per Knopfdruck zu erklären.
Bestellen Sie Ihre kostenlose Videokarte
HIER
° Die Anwendung von Trulicity® erfordert keine Blutzuckerkontrolle durch die Patienten. Allerdings kann eine Eigenkontrolle durch die Patienten notwendig werden, um die Dosis des Sulfonylharnstoffs oder des Insulins anzupassen.1
Trulicity® ermöglicht Ihren Patienten eine nur 1 x wöchentliche und dabei Mahlzeiten unabhängige Anwendung.1 Das kann Ihren Patienten eine höhere Flexibilität im Alltag bieten.
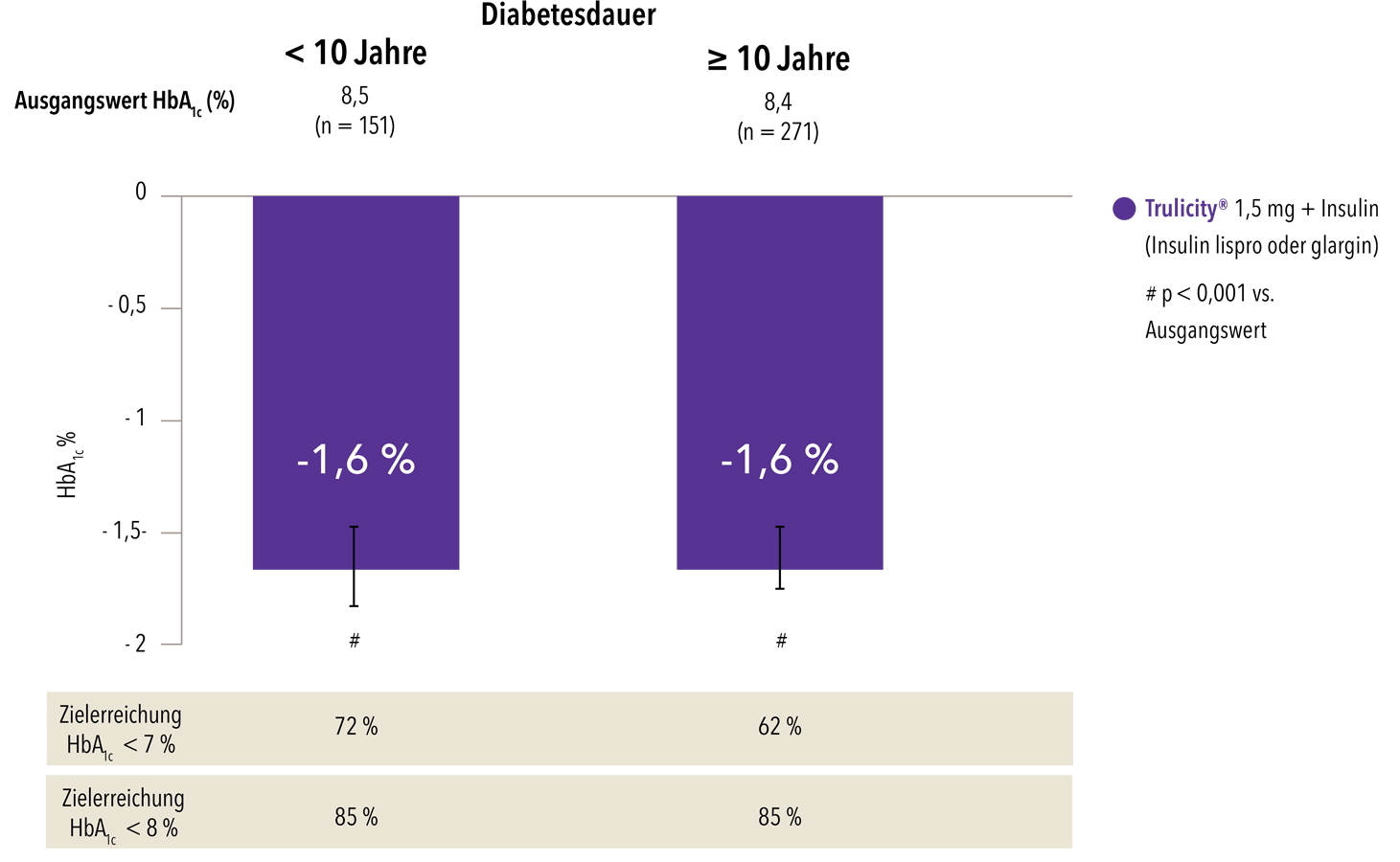
Zusätzlich kann Trulicity® unabhängig von der Diabetesdauer angewendet werden.11
Referenzen
1. Trulicity® Fachinformation. Stand Oktober 2019.
2. Trulicity® Pen-Gebrauchsanweisung. Stand April 2018.
3. Davies MJ et al. Diabetologia. 2018 Dec; 61(12): 2461–2498.
4. Romera I et al. Diabet Med 2019; 36(suppl 1): 169–170.
5. Fuechtenbusch M et al. Diabetes Obes Metab 2019; 21: 1340–1348.
6. Matfin G et al. J Diabetes Sci and Technol 2015; 9(5): 1071–1079.
7. Gerstein HC et al. Lancet 2019; 394(10193): 121–130.
8. Davies MJ et al. Diabetes Care 2018 Dec; 41(12): 2669–2701.
9. Gerstein HC et al., Diabetes Obes. Metab. 2018; 20: 42–49.
10. Giorgino F et al. Diabetes Care. 2015;38(12):2241–2249.
11. Pantalone KM et al. Diabetes Obes Metab. 2018; 20: 1469.
12. Tuttle K. et al. Lancet Diabetes Endocrinol. 2018;6(8):605–617.
13. Dungan KM et al. The Lancet. 2014;384(9951):1349–1357.




