Medizin-Nobelpreis
Verkehrskontrolle in der Zelle
Wie steuern Zellen den Molekülverkehr? Für die Aufklärung erhalten die Forscher Rothman, Schekman und Südhof in diesem Jahr den Medizin-Nobelpreis.
Veröffentlicht:
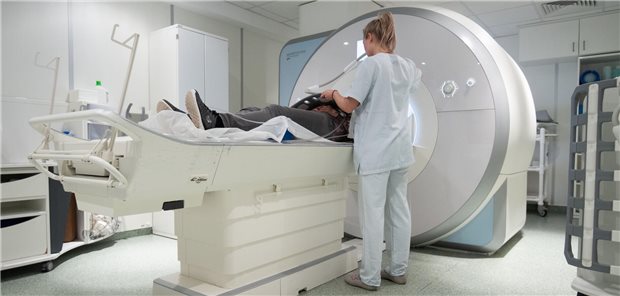
Wie Kalziumionen dafür sorgen, dass an Synapsen Neurotransmitter freigesetzt werden, hat Professor Thomas C. Südhof aufgeklärt.
© Shutterstock
In diesem Jahr erhalten drei Grundlagenforscher der Zellbiologie den Medizin-Nobelpreis, weil es ihnen gelungen ist aufzuklären, wie Zellen es schaffen, den Molekülverkehr in ihrem Innern zu steuern, ohne dass es zu einem Chaos kommt.
Ausgezeichnet werden Professor James E. Rothman von der Yale Universität in New Haven, Professor Randy W. Schekman von der Universität von Kalifornien in Berkeley und Professor Thomas C. Südhof von der Stanford-Universität in Palo Alto.
Der Preis wird ihnen am 10. Dezember in Stockholm verliehen, dem Todestag des Preisstifters Alfred Nobel.
Die Vermutung, dass Kandidaten für den Nobelpreis oft zuvor auch den Albert-Lasker-Preis erhalten haben, hat sich in diesem Jahr wieder einmal bewahrheitet: Erst vor wenigen Wochen wurde Südhof in der Kategorie Medizinische Grundlagenforschung der Lasker-Preis zuerkannt, vor mehr als zehn Jahren in derselben Kategorie Rothman und Schekman.
Und jetzt der Ritterschlag durch die Verleihung des Medizin-Nobelpreises für alle drei Zellbiologen. Sie wurden ausgezeichnet, weil sie entschlüsselten, wie es Zellen gelingt, Hormone, Zytokine, Neurotransmitter und andere Substanzen gefahrlos durch das Zellinnere zu schleusen und schließlich zum richtigen Zeitpunkt und am richtigen Ort aus der Zelle zu entlassen.
Forschungsobjekt Synapsen
Alle drei Wissenschaftler haben Grundlegendes zur Aufklärung der intrazellulären Vorgänge beigetragen. Schekman lieferte durch seine Forschung an der Bäckerhefe vor allem die genetische Basis.
Rothman entdeckte einen Eiweißkomplex, der es einem etwa mit einem Hormon gefüllten Vesikel überhaupt erst ermöglicht, an der richtigen Stelle der Innenseite der Zellmembran anzudocken und schließlich das Hormon aus der Zelle zu entlassen.
Und der Deutsche Südhof, der sich auf die Erforschung von Nervenzellen spezialisiert hat, fand unter anderem heraus, wie es möglich ist, dass Kalziumionen für die rasche Freisetzung von Neurotransmittern aus Synapsen sorgen können.
Zur Erinnerung: Im Zellinnern liegt ein Endomembransystem vor, das aus dem endoplasmatischen Retikulum im Zusammenhang mit dem Golgi-Apparat und seinen Vesikeln besteht. Im endoplasmatischen Retikulum werden Glykoproteine und Lipide der Zellmembran sowie Substanzen synthetisiert, die aus der Zelle ausgeschleust werden sollen.
Aus membranumgrenzten Säckchen, die wie Teller übereinander gestapelt sind, bildet das endoplasmatische Retikulum den Golgi-Apparat, eine Art Weiterverarbeitungs- und Sortieranlage für Proteine. Von dort aus werden diese durch Transportvesikel an ihren Bestimmungsort innerhalb der Zelle gebracht.
Gemeinsame Forschungen
Rothman begreift die intrazellulären Vorgänge wie eine Maschine, in der ein Rädchen ins andere greift, wobei die vielen unterschiedlichen Proteine die Rädchen sind.
Seine Entdeckungen im Laufe der Jahre wurden durch Schekmans Forschungen bestätigt und umgekehrt. Mal forschten sie gemeinsam, mal eher als Konkurrenten, wie Schekman jetzt in einem Interview der Nobelstiftung sagte.
Südhof, den die Nachricht, mit dem Nobelpreis geehrt zu werden, unterwegs zu einer Tagungsreise in Spanien überrascht hat, entdeckte unter anderem, dass das Protein Synaptotagmin innerhalb von synaptischen Vesikeln Kalziumionen bindet.
In Experimenten mit Mäusen konnte er zeigen, dass dem Eiweißmolekül tatsächlich die Rolle eines Kalziumsensors zukommt: Binden die Ionen nach einem elektrischen Signal an das Protein, dockt das Vesikel an die Zellmembran, seine Hülle verschmilzt mit ihr und der Neurotransmitter wird schlagartig nach außen freigesetzt.
Physiologische Prozesse wie die neuronale Kommunikation im Gehirn oder immunologische Reaktionen erfordern also einen reibungslosen Transport von Proteinen durch die Zelle. Fällt ein Rädchen aus, stört das die Ausschüttung etwa von Insulin, von Neurotransmittern oder Zytokinen.
Die nicht normal ablaufende Fusion der Vesikel mit der Zellmembran ist Ursache für eine Reihe von Erkrankungen.
So haben zum Beispiel manche Patienten mit einer bestimmten Form von Epilepsie (infantile epileptische Enzephalopathie) eine Mutation im Gen für das Eiweißmolekül MUNC-18-1. Gemeinsam mit drei anderen Eiweißmolekülen bildet dieses einen Komplex, der für die Vesikelfusion mit der Zellmembran - nicht nur in Synapsen - unentbehrlich ist. Er wird von den Forschern als SNARE-Komplex bezeichnet.
Auch bei der hämophagozytotischen Lymphohistiozytose haben die Patienten, die sehr hohes Fieber und eine vergrößerte Milz haben, Mutationen in Genen wie MUNC, die an Vesikeltransport und -fusion beteiligt sind.
Natürliche Killerzellen können ihre Kontrollfunktion nicht mehr richtig wahrnehmen, was zu ausgeprägten, potenziell tödlich verlaufenden Entzündungsreaktionen führen kann.
Geregelter Proteinverkehr für HIV
Schließlich erklären die von den drei Preisträgern entdeckten Zusammenhänge auch, wie es zu Lähmungserscheinungen nach einer Infektion mit Clostridium botulinum kommt.
Die meisten Toxine dieser anaerob lebenden Bakterien schädigen den zentralen Proteinkomplex und verhindern dadurch, dass Acetylcholin an der motorischen Endplatte ausgeschüttet wird.
Entsprechend macht das Tetanustoxin den Eiweißkomplex funktionslos, sodass in hemmenden Neuronen die Ausschüttung von Gamma-Aminobuttersäure und Glycin, den wichtigsten hemmenden Botenstoffen, unterbleibt.
Und vor zwei Jahren entdeckten Forscher, dass der Aids-Erreger HIV bei seiner Vermehrung im Zellinnern offenbar auf den zentralen Proteinkomplex angewiesen ist.
Besonders erfreut über die Verleihung des Nobelpreises an den deutschen Wissenschaftler ist die Bundesministerin für Bildung und Forschung, Professor Johanna Wanka: "Ich beglückwünsche Thomas C. Südhof zu seinem Nobelpreis für Medizin. Seine Forschung hat wichtige Grundlagen geschaffen, die Ursachen zahlreicher Erkrankungen besser zu verstehen. Diese große Auszeichnung ist zugleich Anerkennung und Ansporn für alle deutschen Wissenschaftler, die sich in der Gesundheitsforschung engagieren."
Die Preisträger
Rothman wurde 1950 in Haverhill im US-Bundesstaat Massachusetts geboren. Nach der Promotion 1976 an der Harvard Medical School forschte er am Massachusetts Institute of Technology (MIT) in Cambridge. Seine Forschung zu Vesikeln begann er nach seinem Wechsel an die Stanford-Universität 1978. 20 Jahre später wechselte Rothman zur Yale-Universität in New Haven, wo er die Abteilung für Zellbiologie leitet.
Schekman, geboren 1948 in St. Paul im US-Staat Minnesota, wurde 1974 an der Stanford-Universität promoviert. Zwei Jahre später setzte er seine Forschungen an der Universität von Kalifornien in Berkeley fort, wo er derzeit in der Abteilung für Molekular- und Zellbiologie arbeitet. Zudem forscht er am Howard Hughes Medical Institute in Berkeley.
Südhof wurde 1955 in Göttingen geboren, wo der 1982 zum Dr. med. promoviert wurde. 1983 wechselte er an das University of Texas Southwestern Medical Center in Dallas. Seit 1991 forscht er am Howard Hughes Medical Institute, wo er 2008 zum Professor für Molekulare und Zelluläre Physiologie ernannt.