Bewerber für Galenus-Preis
Kymriah® – anhaltende Remissionen bei fortgeschrittenen B-Zell-Erkrankungen
Tisagenlecleucel (Kymriah®) von Novartis ist eine gegen das Antigen CD19 gerichtete Immunzelltherapie mit autologen, gentechnisch veränderten T-Zellen. Langzeitanalysen der Zulassungsstudien belegen eine kontinuierlich gute Wirksamkeit mit dauerhaftem Ansprechen bei fortgeschrittener akuter B-Zell-Leukämie und diffus großzelligem B-Zell-Lymphom.
Veröffentlicht: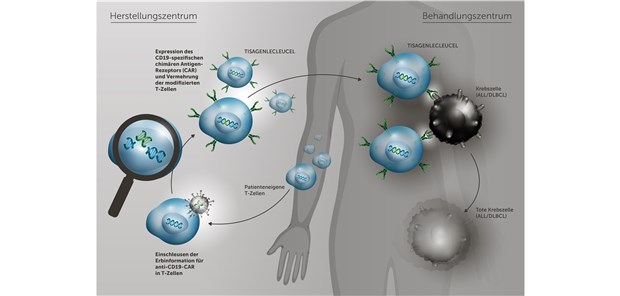
Sowohl Patienten mit Lymphomen als auch mit Leukämien können oft sehr erfolgreich in kurativer Intention behandelt werden. Dies trifft beispielsweise bei der pädiatrischen akuten lymphatischen B-Zell-Leukämie (ALL) und dem diffus großzelligen B-Zell-Lymphom (DLBCL) zu. Versagen die üblichen Therapieformen allerdings, ist die Prognose der Patienten äußerst schlecht. So haben Kinder, Jugendliche und junge Erwachsene mit refraktärer oder rezidivierter (r/r) B-Zell-ALL in der Regel nur noch eine sehr kurze Lebenserwartung von drei bis acht Monaten. Aber auch bei erwachsenen Patienten mit DLBCL, die auf die primäre Therapie nicht ansprechen oder die nach zwei oder mehr Therapielinien ein Rezidiv entwickeln, ist die Prognose mit einem medianen Gesamtüberleben von sechs bis sieben Monaten trotz weiterer chemotherapeutischer Behandlung extrem schlecht. Der Bedarf an wirksamen Therapien für Patienten mit r/r B-Zell-ALL oder DLBCL ist daher erheblich.
Mit der individualisierten CAR (Chimärer Antigen-Rezeptor)-T-Zelltherapie Tisagenlecleucel (Kymriah®) von Novartis, die seit September 2018 in Deutschland verfügbar ist, haben diese Patienten jetzt eine Chance auf Heilung.
Individuell hergestellte Therapie
Zugelassen ist Tisagenlecleucel für die Behandlung von Kindern, Jugendlichen und jungen erwachsenen Patienten im Alter bis zu 25 Jahren mit r/r B-Zell-ALL (Rezidiv nach Transplantation oder zweites oder späteres Rezidiv) sowie zur Behandlung von erwachsenen Patienten mit r/r DLBCL nach zwei oder mehr Linien einer systemischen Therapie.Für die CAR-T-Zelltherapie werden dem Patienten zunächst T-Zellen durch Leukapherese entnommen. Anschließend wird im Labor mittels eines lentiviralen Vektors die DNA-Sequenz für einen CAR in das Erbgut der T-Zellen eingebracht. Der CAR integriert sich in die Zellmembran der T-Zellen, die damit zu sogenannten CAR-T-Zellen werden. Nach einer lymphodepletierenden Chemotherapie werden die umprogrammierten Zellen dem Patienten zurückinfundiert, wo sie sich weiter vermehren und somit den Krebs dauerhaft bekämpfen. Im Körper des Patienten vermittelt der CAR eine spezifische Bindung an das Oberflächenantigen CD19, das sich unter anderem auf den Tumorzellen befindet. Diese Bindung geht mit einer Aktivierung der jeweiligen CAR-T-Zelle einher. Auf diese Weise werden die CAR-T-Zellen in die Lage versetzt, die malignen Zellen des Patienten zu erkennen und zu eliminieren. Die vollständige Aktivierung der CAR-T-Zelle wird mithilfe der kostimulatorischen Signaldomäne 4-1BB vermittelt, die zu einer lange anhaltenden Persistenz der CAR-T-Zellen im Körper und damit zu einer gesteigerten antitumoralen Antwort führt.
Langfristige Remissionen erzielt
Zugelassen wurde Tisagenlecleucel in den beiden Indikationen r/r B-Zell-ALL und r/r DLBCL auf Basis der zentralen klinischen Studien ELIANA und JULIET. Aus beiden multizentrischen Studien liegen mittlerweile Langzeitdaten vor. Diese belegen für die einmal zu verabreichende, individualisierte CAR-T-Zelltherapie eine kontinuierliche gute Wirksamkeit mit dauerhaftem Ansprechen und ein konsistentes Sicherheitsprofil.Die Langzeitdaten aus der Studie ELIANA belegen für Tisagenlecleucel bei pädiatrischen Patienten mit r/r B-Zell-ALL ein anhaltendes Ansprechen bei den meisten Patienten. Die Remissionsrate betrug 82 Prozent drei Monate nach der Infusion. Das rezidivfreie Überleben nach 24 Monaten betrug 62 Prozent, die mediane Remissionsdauer und das mediane Gesamtüberleben blieben unerreicht.
Bei 98 Prozent der Patienten mit Komplettremission oder Komplettremission mit unvollständiger hämatologischer Erholung, die auf die Behandlung angesprochen hatten, konnte keine minimale Resterkrankung im Knochenmark mehr nachgewiesen werden. Die Gesamtüberlebensrate betrug nach 24 Monaten im Mittel 66 Prozent.
Die Analyse der Langzeitdaten zur CAR-T-Zelltherapie in der JULIET-Studie bei Patienten mit r/r DLBCL ergab, dass die Wahrscheinlichkeit, rezidivfrei zu bleiben, nach sechs Monaten 66 Prozent betrug und im Untersuchungszeitraum nach zwölf und 18 Monaten konsistent bei 64 Prozent blieb. Das mediane Gesamtüberleben nach Tisagenlecleucel-Infusion betrug 11,1 Monate und wurde von Patienten mit einer Komplettremission bislang nicht erreicht. Die Wahrscheinlichkeit des Gesamtüberlebens betrug nach zwölf Monaten 48 Prozent und nach 18 Monaten 43 Prozent.
Die in den Langzeitanalysen aus den Studien ELIANA und JULIET beobachteten Sicherheitsprofile der CAR-T-Zelltherapie stimmten mit den bereits bekannten Ergebnissen aus den Zulassungsstudien überein, therapiebedingte Todesfälle traten nicht auf. (wed)