Moderne Wundversorgung
Bundesrat will Wundprodukte-Branche längere Übergangsfrist gewähren
Unter Corona-Bedingungen können Hersteller sonstiger Wundprodukte dem GBA keineswegs binnen 12 Monaten einen Nutzennachweis erbringen, argumentiert der Bundesrat – und räumt eine verlängerte „Schonfrist“ ein.
Veröffentlicht: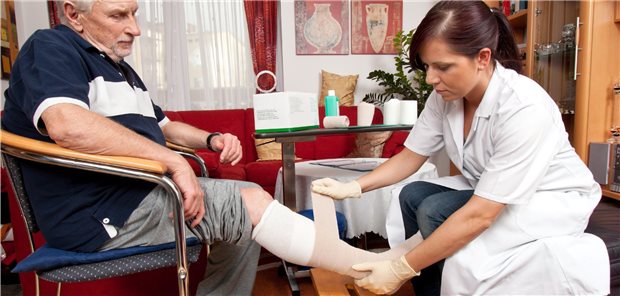
Geht das noch auf Kasse? Bestimmte Wundversorgungslösungen sind seit einem GBA-Beschluss vom 2. Dezember aus der Erstattung gefallen.
© Gina Sanders / stock.adobe.com
Berlin. Beim Gesundheitsausschuss des Bundesrates haben Anbieter moderner Wundversorgungsprodukte offenbar Gehör gefunden in puncto silber- oder PHMB-haltiger Wundauflagen. Nach einem entsprechenden Beschluss des Gemeinsamen Bundesausschusses (GBA) vom 2. Dezember 2020 haben die Anbieter innovativer Wundversorgungslösungen für bestimmte silber- oder PHMB-haltige Wundauflagen ein Jahr Zeit, dem GBA gegenüber einen Nutzennachweis zu erbringen, um die Produkte in der Erstattungsfähigkeit zu halten. Knackpunkt: Die Branche empfindet die Zeit als zu kurz, zumal unter Umständen klinische Studien durchgeführt werden müssten, was per se schon ambitioniert sei in diesem Zeitrahmen, aber unter Corona-Bedingungen schlicht undenkbar.
Beim Bundeskabinett schlugen sich die Bedenken der Wundversorger in einer 24-monatigen Frist für die Erbringung des Nutzennachweises nieder, was im verabschiedeten Gesetzentwurf zum Gesundheitsversorgungsweiterentwicklungsgesetz (GVWG) enthalten ist.
Der Gesundheitsausschuss des Bundesrats empfiehlt in seiner aktuellen Stellungnahme zum GVWG-Entwurf nun, die Übergangsfrist von 24 auf 36 Monate zu verlängern. Begründung: „Aufgrund der Corona-Pandemie ist die Durchführung von klinischen Studien jedoch fast unmöglich. Erst frühestens gegen Ende dieses Jahres kann wieder mit einer gewissen Art von Normalität im Versorgungsalltag gerechnet werden. Erst dann kann generell wieder mit der Durchführung von klinischen Studien in der ambulanten Wundbehandlung mit in der Regel älteren, multimorbiden Wundpatienten begonnen werden. Zu diesem Zeitpunkt werden aber bereits mindestens 12 Monate der dann jetzt vorgesehenen 24-monatigen Übergangsfrist verstrichen sein. Demnach hätten die betroffenen Hersteller also erneut nur eine 12-monatige Übergangsfrist zur Umsetzung zur Verfügung.“
Der Bundesrat berät in seiner Sitzung am 12. Februar über die Ausschussempfehlung. Vermutlich wird das Bundeskabinett am 24. Februar eine Gegenäußerung zur Bundesratsstellungnahme verabschieden. Das GVWG geht dann Ende Februar/Anfang März in den Deutschen Bundestag.