EU-Kommission
EU plant neue Regeln für Blut- und Gewebespenden
EU-weit soll mehr Patientinnen und Patienten Zugang zu benötigten Behandlungen mit Blut- und Gewebespenden ermöglicht werden – unabhängig von ihrem Wohnort. Dazu hat die EU-Kommission einen Vorschlag für neue Regeln entwickelt.
Veröffentlicht: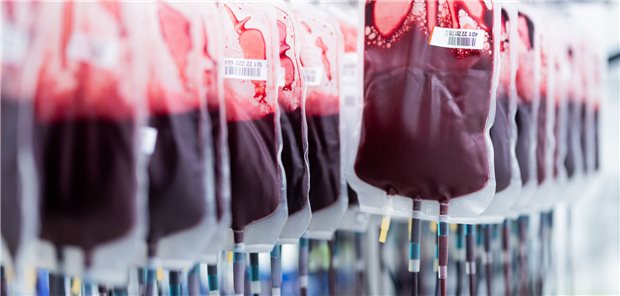
Blut spenden in der Europäischen Union soll künftig sicherer werden. Dazu hat die EU-Kommission neue Regeln für Blut- und Gewebespenden vorgeschlagen.
© Rolf Vennenbernd/dpa
Brüssel. Blut spenden in der Europäischen Union soll künftig sicherer werden. Die EU-Kommission schlug am Donnerstag neue Vorschriften für das Spenden und Empfangen lebenswichtiger Substanzen menschlichen Ursprungs vor. Dazu sollen neben Blut unter anderem auch Gewebe, Zellen oder Muttermilch gehören.
„Ziel ist es, EU-weit mehr Patientinnen und Patienten Zugang zu benötigten Behandlungen zu ermöglichen, und zwar unabhängig von ihrem Wohnort“, teilte die EU-Kommission mit. Der grenzüberschreitende Austausch der Therapien solle erleichtert sowie einheitlich hohe Qualitäts- und Sicherheitsstandards gewährleistet werden. Die neuen Regeln sollen Richtlinien von 2002 beziehungsweise 2004 ersetzen.
Ausweitung auf Muttermilch
Seitdem seien einerseits neue Bedrohungen durch Infektionskrankheiten entstanden, andererseits hätten sich die Technologien für die Verarbeitung von Blut, Geweben und Zellen weiterentwickelt, teilte die EU-Kommission mit. Zudem seien der Gesundheitsschutz der Spender bislang nicht ausreichend berücksichtigt und die Vorgaben nicht EU-weit einheitlich angewendet worden.
Vom neuen Vorschlag werden alle Substanzen menschlichen Ursprungs mit Ausnahme fester Organe erfasst. Unter anderem sollen die Regeln auf Muttermilch ausgeweitet werden. Auch sollten Spender und Empfänger etwa von Transfusionen und Transplantaten sowie Nachkommen aus künstlicher Befruchtung besser geschützt werden.
Gemeinsames Verfahren zur Bewertung und Zulassung
Nationale Aufsichtsbehörden sollen etwa mit Schulungen von der EU unterstützt werden. Innovationen sollen dadurch gefördert werden, dass ein „gemeinsames Verfahren zur Bewertung und Zulassung“ der Präparate aus menschlichen Substanzen geschaffen wird. Alle Stellen, die für die Sicherheit und Qualität der Präparate relevant sind, sollen sich künftig registrieren müssen.
Nun müssen sich das EU-Parlament und die EU-Staaten auf eine Position zu dem Vorschlag der EU-Kommission verständigen, ehe sie über eine gemeinsame Linie verhandeln. (dpa)