Kritik von der Industrie
AMNOG mit Sand im Getriebe
Mit der Einführung der frühen Nutzenbewertung hat Deutschland eine europäische Entwicklung nachgeholt. Im Detail gibt es am Verfahren noch Einiges zu feilen, findet ein Industrievertreter.
Veröffentlicht: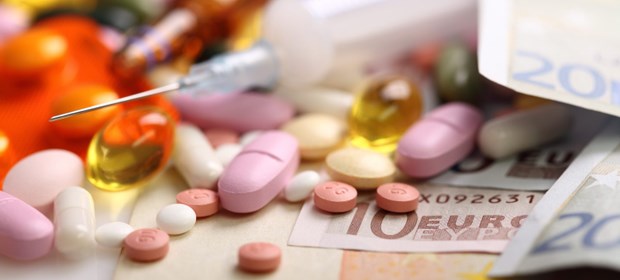
Zwischen Arzneipreis und Zusatznutzen.
© Sven Bähren / fotolia.com
BERLIN. Die Ermittlung des Zusatznutzens einer Arznei vom Preis der zweckmäßigen Vergleichstherapie zu lösen, hat Dr. Andreas Kress von Novartis gefordert.
Bei der Wahl der Vergleichstherapie durch das Institut für Qualität und Wirtschaftlichkeit stehe der Preis im Vordergrund, selbst wenn die so ermittelten Vergleichsarzneien für Studienzentren oft uninteressant seien.
Beim 10. Novartis Kolloquium zur Gesundheitsökonomie in Berlin setzte sich der für den Marktzugang von Wirkstoffen verantwortliche Manager des Unternehmens für einen vertretbaren Aufwand des Nutzenbewertungsverfahrens nach dem Arzneimittelmarktneuordnungsgesetz (AMNOG) für alle Verfahrensbeteiligten ein.
Nach wie vor sei es so, dass Unternehmen vom Gemeinsamen Bundesausschuss (GBA) keine ausreichende Beratung einschließlich Hinweisen auf die nachgefragten Studiendesigns erhielten, sagte Kress.
Länderübergreifende Forschungsprogramme gestalteten sich schwierig, wenn der GBA die vom Hersteller gewählten Vergleiche nicht zeitnah anerkenne.
Diese Ausgangslage sorge auch bei den sich an die frühe Nutzenbewertung anschließenden Preisverhandlungen mit den Krankenkassen für eine schwere Verhandlungsposition auf Unternehmensseite. Einzige Option der Hersteller bei einem Scheitern der Verhandlungen sei, ein Arzneimittel vom Markt zu nehmen.
Kress beschrieb aus seiner Sicht einige aus seiner Sicht überflüssige Erschwernisse des Verfahrens. Die ursprüngliche Schätzung des Gesetzgebers, ein Dossier zu erstellen dauere etwa zweieinhalb Tage sei längst Makulatur.
Kommt die Bewertung schon vor der Zulassung?
Die bisher eingereichten Dossiers seien zwischen 292 und 986 Seiten stark, der Arbeitsaufwand dafür entsprechend. Für die anstehenden Bewertungen im Bestandsmarkt gebe es die Vorgabe, auch veraltete Studien übersetzen zu lassen. Der Aufwand dafür betrage zwischen 250.000 und 300.000 Euro.
Trotz der Detailkritik zeigte sich Kress optimistisch, gemeinsam mit dem GBA überflüssige Verfahrenselemente zu identifizieren und aus dem Prozess der frühen Nutzenbewertung zu entfernen.
Oder auch Kompromisse zu finden, wenn idealerweise notwendige Studien nicht durchführbar seien. "Die Tatsache, dass kein Präparat mit einem bestätigten Zusatznutzen in den Preisverhandlungen in die Schiedsstelle musste, spricht für die Verhandlungsqualität", sagte Kress.
Was die frühe Nutzenbewertung angeht, ist Deutschland kein Sonderfall mehr. Die Verfahren in Europa unterschieden sich zwar, die Ergebnisse lägen aber nahe beieinander, sagte Dirk Kars von der Kölner Unternehmensberatung Simon-Kucher & Partners.
Eine Harmonisierung der Nutzenbewertung auf EU-Ebene sei aber langfristig nicht in Sicht. Ein Effekt der Verfahren sei in absehbarer Zeit aber eine Harmonisierung der Arzneimittelpreise.
Die frühe Nutzenbewertung ist inzwischen auch Gegenstand ethischer Überlegungen. Sie schöpfe Wirtschaftlichkeitsreserven aus und steigere somit die allgemeine Wohlfahrt. Deshalb sei das Verfahren ethisch gerechtfertigt, sagte Dr. Oliver Rauprich von der Universität München.
Sein Ausblick: Die Bewertung solle vor der Zulassung erfolgen. Zudem sollten mittelfristig auch indikationsübergreifende Nutzenbewertungen entwickelt werden.







