Roche
So viele Innovationen auf einmal am Start wie noch nie
Für Roche wird 2016 aller Voraussicht nach auch im deutschen Markt wieder ein gutes Jahr. Zwar droht den Schweizern in absehbarer Zeit größere Biosimilar-Konkurrenz. Deren Auswirkung dürfte aber durch jede Menge neue Produkte abgefedert werden.
Veröffentlicht:
Hoch hinaus geht es bei Roche auch im neuen Büroturm am Stammsitz Basel.
© Roche
FRANKFURT/MAIN. Im sechsten Jahr der frühen Nutzenbewertung zieht der Pharmahersteller Roche eine positive AMNOG-Bilanz: Acht Neueinführungen habe man seither in Deutschland absolviert und bislang sieben Verfahren der frühen Nutzenbewertung abgeschlossen. "Alle erfolgreich", betonte bei einem Hintergrundgespräch am Mittwoch in Frankfurt Roche-Deutschland-Chef Dr. Hagen Pfundner.
Das spiegele sich auch in der wirtschaftlichen Situation der hiesigen Landesgesellschaften wider. Nach überdurchschnittlichem Plus im Vorjahr - 2015 verbesserte sich der Umsatz im Geschäft mit Dritten um acht Prozent auf 2,6 Milliarden Euro, während der Pharma-Gesamtmarkt bundesweit nur um knapp sechs Prozent zunahm - halte die gute Wachstumsdynamik weiterhin an, versicherte Pfundner.
Konkurrenz absehbar
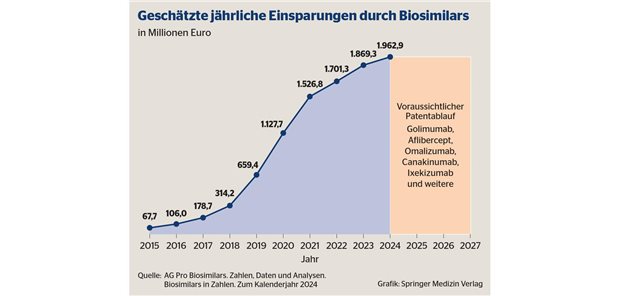
Gleichwohl kann sich auch Roche über mangelnde Herausforderungen nicht beklagen: Spätestens ab Ende kommenden Jahres rechnet Konzernchef Dr. Severin Schwan mit Biosimilar-Konkurrenz für die Krebs-Blockbuster Trastuzumab (Herceptin®) und Rituximab (MabThera®).
Für beide Antikörper sei der europäische Patentschutz bereits abgelaufen. Eigentlich habe er mit dem Markteintritt rekombinanter Nachahmer schon früher gerechnet, so Schwan. Ein generischer Konkurrent sei zwar mit einem Zulassungsdossier vorgeprescht, habe aber den regulatorischen Anspruch unterschätzt. Den weiteren Anbietern, die mit Biosimilars erst jetzt kurz vor der Zulassung stehen - bei der europäischen Arzneimittelagentur EMA sind aktuell zwei Zulassungsanträge für Rituximab-Similars anhängig, jedoch noch keiner für ein Trastuzumab-Analogon -, werde das nicht passieren, ist sich Schwan sicher. Für Roche komme es jetzt darauf an, mit neuen Produkten die drohende Umsatzerosion abzufangen. Das nächste ganz große Konzernprodukt, das die Marktexklusivität verliert, ist ab 2020 der Krebs-Antikörper Bevacizumab (Avastin®).
Nachschub rollt
An neuen Produkten fehlt es jedenfalls nicht. Er sei deshalb "zuversichtlich, die bevorstehende Biosimilarwelle gut zu überstehen", sagte Schwan. Nach Angaben des Konzernchefs ist Roche "in der historisch einmaligen Lage", gleich fünf Produkte in der Einführungsphase oder kurz vor der Zulassung zu haben. Darunter auch die beiden ganz großen Hoffnungsträger Atezolizumab (Tecentriq®, Krebs-Immuntherapie) und Ocrelizumab (Ocrevus®, Anti-CD20-Antikörper gegen sowohl schubförmige als auch primär progrediente MS).
Für beide Wirkstoffe ist die Zulassung in Europa und den USA beantragt, für Atezolizumab in den USA bereits in der Erstindikation Blasenkrebs erteilt. Ocrevus® könnte noch dieses Jahr - und damit früher als geplant - in den US-Markt kommen, hofft Schwan.
Weitere Einführungs-Kandidaten seien das bereits vergangenen November europaweit freigegebene Hautkrebsmittel Cobimetinib (Cotellic®), der noch im Zulassungsverfahren befindliche ALK-Inhibitor Alectinib (Alecensa®) gegen nicht-kleinzelligen Lungenkrebs sowie der orale BCL-2-Inhibitor Venetoclax gegen chronisch lymphatische Leukämie, der in den USA bereits seit April, in Europa dagegen bis dato noch nicht zugelassen ist.