Demenz-Forschung
Entzündungsmechanismen treiben Alzheimer voran
Ein Molekülverbund des Immunsystems – Forscher sprechen von ASC Specks – fördert die Ablagerung von Amyloid-Beta-Peptiden. Ein neuer Ansatz für die Therapie bei M. Alzheimer?
Veröffentlicht: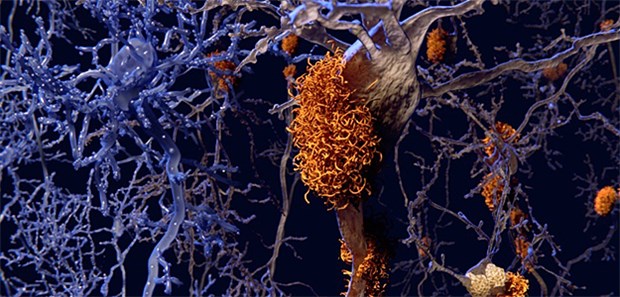
Typisch für Alzheimer: Neurone mit Amyloidplaques (rechts) – hier im Vergleich zu gesunden Neuronen (links)
© selvanegra / Getty Images / iStock
BONN. Entzündungsmechanismen treiben grundlegende Prozesse der Alzheimer-Erkrankung voran, haben Forscher des Deutschen Zentrums für Neurodegenerative Erkrankungen (DZNE) in der Helmholtz-Gemeinschaft und der Universität Bonn beobachtet (Nature 2017; 552: 355–361). Auslöser sei das Immunsystem des Gehirns.
Die Forschungsergebnisse, an denen weitere Wissenschaftler aus Europa und den USA beteiligt waren, könnten auf lange Sicht den Weg für eine frühe Behandlung von Alzheimer-Kranken bereiten: zu einem Zeitpunkt, zu dem noch keine Symptome da sind.
Aß-Ablagerungen setzen entzündliche Prozesse in Gang
Im Zuge des Krankheitsprozesses bei Morbus Alzheimer verkleben ja Amyloid-Beta-Peptide, kurz "Aß" genannt, und lagern sich im Gehirn ab, erinnern DZNE und Universität Bonn in einer gemeinsamen Mitteilung zur Veröffentlichung der Studie. Diese Aggregate stehen im Verdacht, Neuronen zu schädigen.
In jüngsten Jahren habe sich zudem herausgestellt, dass Aß-Ablagerungen entzündliche Prozesse in Gang setzen. Angestoßen werden sie vom angeborenen Immunsystem des Gehirns, dessen Repertoire anders als bei der adaptiven Immunabwehr genetisch festgelegt ist. Die Mechanismen, die eine Alzheimer-Erkrankung vorantreiben und Nervenzellen letztlich absterben lassen, wurden im Detail bislang nicht verstanden.
"Die Ablagerung und Ausbreitung von Aß beginnt wahrscheinlich Jahrzehnte bevor erste klinische Symptome auftreten, beispielsweise Störungen des Kurzeitgedächtnisses. Ein besseres Verständnis dieser Prozesse könnte daher ein Schlüssel zu neuartigen Therapie-Ansätzen sein. Hier ginge es darum, Alzheimer im Frühstadium zu behandeln, bevor sich geistige Beeinträchtigungen bemerkbar machen", wird Professor Michael Heneka in der Mitteilung zitiert. Heneka ist Arbeitsgruppenleiter am DZNE und Direktor an der Klinik für Neurodegenerative Erkrankungen und Gerontopsychiatrie des Universitätsklinikums Bonn.
Entzündliche Reaktionskette
Heneka und Kollegen befassen sich schon länger mit der Frage, wie die Immunreaktion des Gehirns die Entwicklung der Alzheimer-Erkrankung beeinflusst, berichten DZNE und Universität Bonn. In früheren Studien hätten sie herausgefunden, dass ein molekularer Sensor des angeborenen Immunsystems – ein Proteinkomplex mit der Bezeichnung NLRP3 – eine Schlüsselrolle hat: Im Gehirn von Alzheimer-Patienten, so zeigte sich, ist NLRP3 aktiviert. Und bei Mäusen mit kognitiven Störungen ähnlich denen von Alzheimer-Patienten ist NLRP3 an der Krankheitsentwicklung beteiligt.
NLRP3 verändert bei Aktvierung seine Struktur und veranlasst das Immunsystem, entzündungsfördernde Substanzen herzustellen. Darüber hinaus verbindet sich NLRP3 bei Aktivierung mit dem Eiweißmolekül ASC. Zellen können derlei Aggregate – sie werden "ASC Specks" genannt – ausschütten. "Die Freisetzung von ASC Specks aus aktivierten Zellen konnte man bisher nur bei Fresszellen, den sogenannten Makrophagen, nachweisen. Doch ihre Bedeutung für den Krankheitsprozess war bisher rätselhaft", so Professor Eicke Latz, Leiter des Instituts für Angeborene Immunität und Mitglied des Exzellenzclusters ImmunoSensation der Universität Bonn sowie Forscher am DZNE.
Verbindung zwischen Entzündung und Neurodegeneration
Die aktuellen Untersuchungen zeigen nun, dass ASC Specks auch von aktivierten Immunzellen des Gehirns – den Mikroglia – freigesetzt werden. Darüber hinaus belegen sie eine molekulare Verbindung zur Neurodegeneration.
"Wir fanden heraus, dass ASC Specks im extrazellulären Raum an Aß binden und die Ablagerung von Aß fördern. Das trägt direkt zum Fortschreiten der Pathologie und damit zur Krankheitsentwicklung bei", so Heneka in der Mitteilung von DZNE und Universität Bonn.
Neuer Ansatz für die Therapie?
Diese Einschätzung stützt sich auf eine Reihe von Experimenten mit Mausmodellen der Alzheimer-Krankheit. Die Forscher untersuchten dabei die Wirkung der ASC Specks sowie die ihres Bestandteils, des Proteins ASC auf die Ausbreitung von Aß-Ablagerungen im Gehirn.
"In unserer Studie haben wir zudem durch Analysen von menschlichem Hirngewebe gezeigt, dass Entzündungsreaktionen und Aß-Pathologie beim Menschen in ähnlicher Weise ineinandergreifen können. Zusammenfassend legen unsere Ergebnisse nahe, dass Entzündungen des Gehirns nicht nur eine Begleiterscheinung der Alzheimer-Krankheit sind. Sie tragen vielmehr dazu bei, dass die Erkrankung voranschreitet", wird Heneka zitiert. "Eine Beeinflussung dieser Immunantwort könnte daher neue Möglichkeiten auftun, Alzheimer zu behandeln." (eb)