FDA / USA
Erste reguläre Remdesivir-Zulassung gegen COVID-19
Aufgrund dreier klinischer Studien mit insgesamt rund 2000 Teilnehmern sieht die FDA die Wirksamkeit des Virushemmers Remdesivir gegen COVID-19 unter Beweis gestellt.
Veröffentlicht: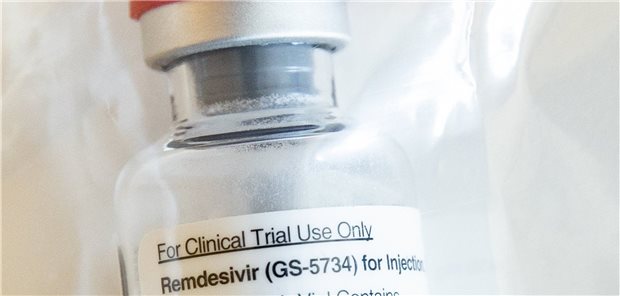
Eine Ampulle des Medikamentes Remdesivir.
© Ulrich Perrey / dpa
Silver Spring. Die US-Zulassungsbehörde FDA hat am Donnerstag Gileads Veklury® (Remdesivir ) gegen COVID-19 zugelassen. Dabei handelt es sich den Angaben zufolge um die erste reguläre Genehmigung für ein COVID-Medikament in den USA. Sie gilt für hospitalisierte Erwachsene und Kinder ab 12 Jahren und 40 Kilogramm Körpergewicht.
Wie die Behörde betont, beinhaltet diese reguläre Zulassung nicht den Gebrauch bei Patienten, den die bereits früher erteilte und jetzt aktualisierte Notfallerlaubnis („Emergency Use Authorization“) für Remdesivir vorsieht. Danach darf der Wirkstoff in Ermangelung anderer Optionen auch bei hospitalisierten pädiatrischen COVID-19-Patienten gegeben werden, die zwischen wenigstens 3-5 und 40 Kilogramm wiegen. Umfassende klinische Daten zur Sicherheit und Wirksamkeit in dieser Subgruppe müssten aber noch beigebracht werden, so die FDA.
„Meilenstein in der Pandemie“
Behördenchef Stephen Hahn kommentiert die Remdesivir-Zulassung als „wichtigen wissenschaftlichen Meilenstein in der COVID-19-Pandemie“. Etwaigen Spekulationen, die Behörde könnte sich politischem Druck zugunsten einer schnellen Freigabe gebeugt haben, kommt Hahn mit dem Hinweis zuvor, man habe sich die klinischen Studiendaten gründlich angesehen („rigorously assessed“).
Wie es in der Mitteilung weiter heißt, liegen der FDA-Zulassung drei klinische Studien zugrunde: An einem placebokontrollierten Doppelblindtest nahmen 1062 Probanden teil, die milde, mittelschwere und schwere Symptome zeigten. In zwei weiteren Open-label-Studien wurde Remdesivir einmal in sowohl fünf- als auch zehntägiger Gabe gegen die Standardtherapie geprüft, das andere Mal die fünftägige Gabe mit der zehntägigen verglichen. An diesen offenen Versuchen nahmen knapp 1000 Probanden teil.
Die mediane Zeit bis zur Rekonvaleszenz im Verum-Arm der RCT-Studie betrug demnach zehn Tage, in der Placebogruppe 15 Tage; Rekonvaleszenz war definiert als Krankenhausentlassung oder erfolgreiches Absetzen der Sauerstoffzufuhr sowie weiterer medizinischer Behandlungsmaßnahmen. Daten zur Mortalität werden in der FDA-Mitteilung nicht erwähnt. (cw)