Preisbildungsverfahren bei Onkologika und Orphan Drugs
Nutzenbewertung bei Krebsmedikamenten: Nötig ist Nachsteuern im Detail
Veränderungen am AMNOG-Verfahren: Die Preisbildung bei Onkologika und Orphan Drugs steht für GBA und Kassen auf dem Wunschzettel an die nächste Bundesregierung.
Veröffentlicht:
Angesichts des Add-on-Effekts der Kosten bei Kombinationstherapien sehen GBA und Kassen den Gesetzgeber gefordert.
© Scanrail / stock.adobe.com
Berlin. Der Gemeinsame Bundesausschuss und Krankenkassen erwarten, dass der Gesetzgeber in der nächsten Legislaturperiode das Preisbildungsverfahren für Arzneimittel mit neuen Wirkstoffen modifizieren sollte. Im Blickpunkt stehen dabei Onkologika und Orphan Drugs.
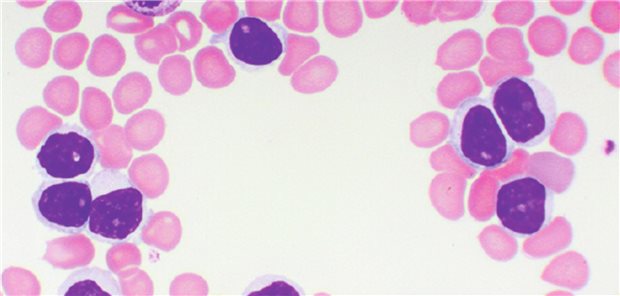
Krebstherapeutika machen nach Angaben des GBA-Vorsitzenden Professor Josef Hecken bei der Handelsblatt-Tagung Pharma 2021 1,1 Prozent der Verordnungen aus, absorbieren aber 18,7 Prozent der GKV-Arzneimittelausgaben. Das Problem sei, dass neue Wirkstoffe nicht alte ersetzen, sondern zusätzlicher Therapiepartner in einer Kombinationstherapie werden. Aufgrund des Add-on-Effekts komme es dann zu einer Verdoppelung der Therapiekosten. Die Bildung der Erstattungsbeträge nach der frühen Nutzenbewertung findet isoliert für jeden einzelnen Wirkstoff statt – die Gesamtbehandlungskosten bleiben außer Betracht und können nicht verhandelt werden, so Hecken. Hier wäre der Gesetzgeber gefordert.
Moderate Weiterentwicklung nötig
„Moderate Weiterentwicklungen“ für den Erstattungsbetrags-Mechanismus, der seit 2011 unverändert geblieben ist, hält auch Dr. Ulf Maiwald, Leiter der Arzneimittelversorgung der AOK Plus, für erforderlich. Korrekturbedarf sieht er bei Orphan Drugs und ihrem bevorzugten Status für den Fall, dass es in einem Indikationsgebiet mehrere Orphan Drugs gibt.
Dann sollte der Zusatznutzen nicht mehr automatisch anerkannt werden, sondern ein komplettes Nutzenbewertungsverfahren angesetzt werden. In der Onkologie stehe die Nutzenbewertung vor dem Dilemma, dass bei Kombinationstherapien der therapeutische Beitrag eines einzelnen Kombinationspartners nicht isoliert werden kann.
18,7 Prozent der Arzneiausgaben in der GKV werden durch die Verordnung von Onkologika absorbiert. Dabei handelt es sich aber nur um 1,1 Prozent der Verordnungen insgesamt, sagt der unparteiische GBA-Vorsitzende Professor Josef Hecken.
Im Zusammenhang mit der jüngst gestarteten anwendungsbegleitenden Datenerhebung für Arzneimittel mit beschleunigter Zulassung und geringer Studienevidenz forderte Hecken die Hersteller auf, spätestens sechs Monate von der geplanten Markteinführung und noch vor der Zulassung mit dem GBA Kontakt aufzunehmen.
Datenerhebung geht nicht „in Serie“
Die unkontrollierte Markteinführung von Zolgensma® bezeichnete Hecken als „Negativbeispiel“, bei dem es der Hersteller verabsäumt habe, den GBA zu kontaktieren. Die Folge sei, dass es zu einer Behandlung von Kindern gekommen sei, deren Daten nicht erhoben würden. Der GBA strebe auch eine enge Abstimmung mit den Zulassungsbehörden an, um deren Auflagen zu berücksichtigen.
Derzeit, so Dr. Antje Behring, die beim GBA für die frühe Nutzenbewertung federführend ist, sind konkret keine weiteren anwendungsbegleitenden Datenerhebungen geplant. Zunächst wolle man die Erfahrungen im Zusammenhang mit Zolgensma® abwarten. Aus ihrer Sicht werde das Instrument der Datenerhebungen zur Generierung besserer Evidenz etwa durch systematische krankheitsbezogene Registerstudien nicht in Serie gehen und auf wenige unter besonderen Umständen zugelassene Arzneimittel beschränkt bleiben.