Bewerber für Galenus-Preis 2019
Yescarta®– personalisierte T-Zelltherapie bei fortgeschrittenen B-Zell-Lymphomen
Axicabtagen-Ciloleucel (Yescarta®) von Kite und Gilead ist eine gegen das Antigen CD19 gerichtete Immuntherapie mit genetisch modifizierten autologen T-Zellen. Die neue Therapieoption mit kurativem Potenzial wird bei Patienten mit rezidivierten oder refraktären aggressiven großzelligen B-Zell-Lymphomen eingesetzt.
Veröffentlicht: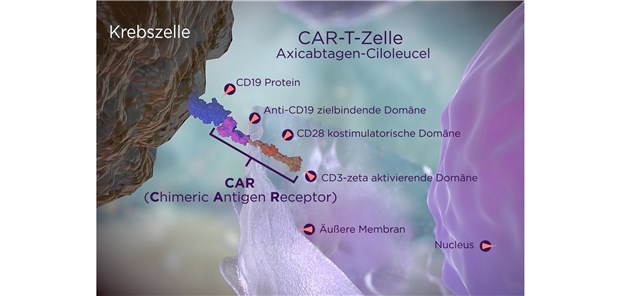
B-Zell-Lymphome zählen zu den häufigsten malignen Neubildungen des lymphatischen Systems. Die Prognose der Non-Hodgkin-Lymphome (NHL) ist mit einer relativen Fünf-Jahres-Überlebensrate von über 60 Prozent insgesamt eher gut, die Behandlung besteht je nach Schwere der Erkrankung in der Regel in einer Strahlen- oder Chemotherapie. Kommt es bei den Betroffenen jedoch zu einem Rückfall oder sprechen sie nicht auf die Standardtherapien an, verschlechtern sich ihre Heilungschancen rapide. Wie die Ergebnisse einer retrospektiven Metaanalyse belegen, ist zum Beispiel die Prognose von Patienten mit refraktärem, diffus großzelligem B-Zell-Lymphom mit einem medianen Gesamtüberleben von 6,3 Monaten und einer Zwei-Jahres-Überlebensrate von lediglich 20 Prozent sehr schlecht.
Infolgedessen besteht für Patienten mit refraktärem oder rezidivierendem Non-Hodgkin-Lymphom erheblicher Bedarf an neuen, effektiveren Therapien. Dies gilt ebenso für Patienten mit Rezidiv nach einer autologen Stammzelltransplantation (ASZT), für Patienten, die für eine ASZT ungeeignet sind, sowie für Patienten, die auch für eine allogene Stammzelltransplantation ungeeignet sind.
Zelluläre Immuntherapie
Axicabtagen-Ciloleucel (Yescarta®) von Kite und Gilead ist eine neue, personalisierte Zelltherapie, die seit Oktober 2018 in Deutschland zur Verfügung steht. Sie bietet schwerkranken Lymphom-Patienten die Chance auf Heilung. Zugelassen ist Axicabtagen-Ciloleucel zur Behandlung erwachsener Patienten mit rezidiviertem oder refraktärem diffus großzelligem B-Zell-Lymphom (DLBCL) und primär mediastinalem großzelligem B-Zell-Lymphom (PMBCL) nach zwei oder mehr systemischen Therapien.Für die Therapie mit Axicabtagen-Ciloleucel werden dem Patienten durch Leukapherese Leukozyten entnommen, die T-Zellen isoliert und mittels retroviraler Transduktion so modifiziert, dass sie einen chimären Antigen-Rezeptor (CAR) exprimieren. Dieser umfasst ein variables Maus-Anti-CD19-Einzelkettenfragment (scFv, Ziel-bindende Domäne), das über eine Transmembran-Domäne mit der kostimulatorischen CD28-Domäne und der CD3-zeta-aktivierenden Domäne verbunden ist. Die gentechnisch modifizierten CAR-T-Zellen werden anschließend vermehrt und dem Patienten re-infundiert.
Mittels dieses CAR richten sich die re-infundierten T-Zellen (sogenannte Anti-CD19-CAR-positive T-Zellen) gegen CD19, ein Oberflächenmolekül von B-Lymphozyten. Nach der Bindung der Anti-CD19-CAR-positiven T-Zellen an die CD19-exprimierenden Zielzellen werden Signalkaskaden aktiviert, die bei den T-Zellen zu Aktivierung, Proliferation, Akquisition von Effektorfunktionen und Sekretion von inflammatorischen Zytokinen und Chemokinen führen. Diese Abfolge von Ereignissen resultiert in der Apoptose und Nekrose der CD19 exprimierenden Zielzellen.
Hohe Chance auf Langzeitüberleben
Axicabtagen-Ciloleucel wurde auf Basis von Daten aus der offenen, multizentrischen, einarmigen Phase-I/II-Studie ZUMA-1 zugelassen. In der Studie erhielten insgesamt 108 Patienten mit rezidiviertem oder refraktärem B-Zell-NHL die personalisierte Zelltherapie. Die Wirksamkeit wurde in Phase II bei 101 Patienten mit histologisch bestätigtem DLBCL, primär mediastinalen großzelligen B-Zell-Lymphomen (PMBCL) oder aus einem follikulären Lymphom entstandenen DLBCL untersucht. Die Patienten hatten bereits zwei oder mehr systemische Vortherapien erhalten.Für die Phase-I/II-Teile der Studie liegen mittlerweile Zwei-JahresDaten vor. Von den 101 Patienten des Phase-II-Teils der Studie zeigten 83 Prozent ein objektives Therapieansprechen, und bei 58 Prozent wurde eine Komplettremission beobachtet. Die mediane Dauer des Ansprechens betrug 11,1 Monate. Das progressionsfreie Überleben für alle 108 behandelten Patienten lag für die Gesamtgruppe bei median 5,9 Monaten, für Patienten mit Komplettremission war es noch nicht erreicht.
Bei 23 von den 60 Patienten, die einen Monat nach der Infusion kein vollständiges Ansprechen auf Axicabtagen-Ciloleucel gezeigt hatten, war es nach bis zu 15 Monaten doch noch zu einer Komplettremission gekommen. Das mediane Gesamtüberleben war nach einer medianen Nachbeobachtungszeit von 27,1 Monaten noch nicht erreicht. Nach zwei Jahren waren noch 39 Prozent der Patienten krankheitsfrei.
Neurologische Toxizitäten wurden bei 64 Prozent der Patienten beobachtet, dabei bei 28 Prozent vom Grad ≥ 3. Ein Zytokin-Freisetzungssyndrom (CRS) trat bei 93 Prozent der Patienten auf. Das CRS und die neurologischen Nebenwirkungen waren bei 98 Prozent der Patienten reversibel. Im Zwei-Jahres-Follow-up wurden schwere unerwünschte Ereignisse kaum noch beobachtet. (wed)