Corona-Vakzine
Zweiter COVID-19-Impfstoffkandidat in klinischer Prüfung
Auch CureVac kann mit der klinischen Prüfung seines Impfstoffkandidaten gegen COVID-19 beginnen. Gerade einmal 14 Tage brauchte das Paul-Ehrlich-Institut, um sich für eine Zulassung zu entscheiden.
Veröffentlicht: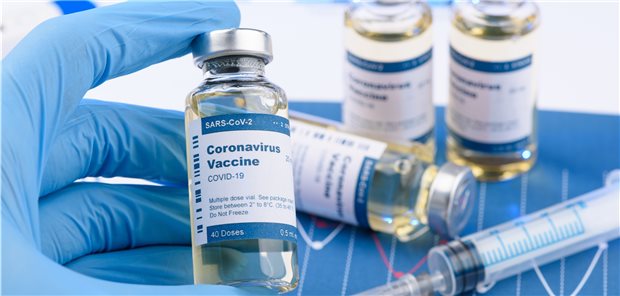
Weltweit befinden sich aktuell zehn Impfstoffkandidaten in der klinischen Prüfung, zwei davon schon in Phase II/III (Symbolbild).
© Dmytro S/stock.adobe.com
Tübingen / Langen. Mit CureVac schickt ein zweites Unternehmen einen COVID-19-Impfstoffkandidaten in Deutschland ins Rennen. Die Zulassung für die klinische Prüfung des mRNA-Impfstoffs „CVnCoV“ in einer Phase-I-Studie gab CureVac heute gemeinsam mit dem Paul-Ehrlich-Institut (PEI) bekannt. Erst kürzlich wurde der erste COVID-19-Impfstoffkandidat des Unternehmens BioNTech in Deutschland zur klinischen Prüfung zugelassen, auch hierbei handelt es sich um einen mRNA-Impfstoff.
Noch im Juni will CureVac nun mit der klinischen Prüfung beginnen, mit ersten Daten rechnet das Unternehmen im September oder Oktober 2020. Die Zulassung könnte bei erfolgreicher klinischer Erprobung schon im Frühjahr 2021 erfolgen, möglicherweise auch bereits zu Beginn des kommenden Jahres.
Studie läuft über 15 Monate
CVnCoV enthält die Bauanleitung für das Spike (S)-Protein – mit dem das Virus an seine Zielzellen bindet – in stabilisierte Prä-Fusionskonformation. In einer teilweise verblindeten, placebokontrollierten Dosis-Eskalationsstudie an vier Testzentren in Deutschland und Belgien soll die Vakzine nun 144 Probanden verabreicht werden, zudem erhalten 24 Studienteilnehmer ein Placebo, wie Dr. Franz-Werner Haas von CureVac berichtete.
Dabei sollen drei unterschiedliche Impfdosen auf Wirksamkeit und Sicherheit untersucht werden. So erhalten je 48 Probanden eine 2 μg Dosis, eine 4 μg Dosis oder eine 6 μg Dosis an Tag 1 und an Tag 29. Unter den Teilnehmern sollen sowohl seropositive als auch seronegative Probanden sein, Risikopersonen werden nicht eingeschlossen. Das Alter der Teilnehmer liegt zwischen 18 und 40 beziehungsweise 41 und 60 Jahren.
Anschließend werden die Teilnehmer ein Jahr lang überwacht, insgesamt werde die Studie über 15 Monate laufen, so Haas. In dieser Zeit könnten bei positiven Daten allerdings bereits Phase-II- und -III-Studien parallel beginnen, um die Zulassung zu beschleunigen so PEI-Präsident Professor Klaus Cichutek.
Hohe Immunogenität im Tiermodell
In In-vivo-Versuchen mit Mäusen hatte sich der Impfstoffkandidat zuvor als immunogen erwiesen, und zwar bereits in einer Dosis von 2 μg. In dieser Dosierung induzierte die Vakzine einen ausreichend hohem Titer von IgG1- und IgG2a-Antikörpern, die zudem SARS-CoV-2 effektiv neutralisieren konnten. Wichtig sei auch, dass durch den Impfstoff eine hohe Frequenz multifunktionaler CD4- und CD8-T-Zellen ausgelöst worden sei, was für die Ausbildung eines guten Immungedächtnisses und damit für einen guten und längerfristigen Impfschutz spreche, berichtete Dr. Mariola Fotin-Mleczek von CureVac.
Corona-Impfstoff
Bund steigt mit 300 Millionen bei CureVac ein
Cichutek wies darauf hin, dass für die Produktion des Kandidaten eine von CureVac entwickelte Impfstoff-Plattform verwendet werde, die eine TH1-gerichtete Immunantwort auslöse und damit unerwünschten Wirkungen vorbeuge. Dies seien bei Impfungen vor allem die Induktion infektionsverstärkender Antikörper und eine TH2-gerichtete Immunantwort mit der Folge von Organschäden.
Unternehmen baut Produktionskapazitäten aus
Derzeit verfüge das CureVac über eine Produktionskapazität von mehreren Millionen Dosen im Jahr, da Ende des vergangenen Jahres eine bereits GMP-qualifizierte Anlage ausgebaut worden sei, so Haas. Eine weitere Produktionsanlage werde aktuell gebaut, deren Fertigstellung auch die EU-Kommission unterstütze. Diese könne die Kapazitäten noch einmal auf Milliarden Impfdosen steigern, nach Zulassung plant CureVac bei Markteinführung mit über 100 Millionen Impfdosen.
Ob sich die mRNA-Technologie grundsätzlich als Methode zur Impfstoffproduktion eignet, ist noch nicht abschließend geklärt: Es gibt bisher keinen einzigen zugelassenen mRNA-Impfstoff. Dennoch ist Cichutek zuversichtlich: „Die Daten sind gut, und negative Langzeitfolgen sind bisher nicht zutage getreten.“